首页 > 醋酸艾替班特注射液说明书
修改日期:2021年4月7日
醋酸艾替班特注射液说明书(Vetter Pharma-Fertigung GmbH & Co.KG)
请仔细阅读说明书并在医师指导下使用
- 【药品名称】
- 通用名称: 醋酸艾替班特注射液
处方药物
【成份】
本品主要成份为醋酸艾替班特。化学名称:(R)-精氨酰-(S)-精氨酰-(S)-丙基-(2 S, 4R)-(4-羟基脯氨酰)甘氨酰-(S)-[3-(2-噻吩基)丙氨酰]-(S)-丝氨酰-(R)-[(1,2,3,4-四氢-3-异喹啉基)甲酰基](2 S, 3aS, 7aS)-[(六氢-2-吲哚啉基)甲酰基]-(S)-精氨酸,醋酸盐
化学结构式:

分子式:C59H89N19O13S· nC2H4O2
分子量:1304.52 · n60.05辅料:氯化钠、冰醋酸、氢氧化钠、注射用水
【适应症】
用于治疗成人、青少年和 ≥ 2 岁儿童的遗传性血管性水肿(HAE)急性发作。
【规格】
3 ml:30 mg(按 C59H89N19O13S 计)
【用法用量】
剂量成人本品的推荐治疗剂量为 30 mg/次,采用腹部皮下缓慢注射方式给药。一般情况下,单次注射足以治疗疾病的一次发作。在不足以缓解或症状复发情况下,可在 6 小时后注射第 2 次。如果第 2 次注射产生的疗效不足以缓解症状或症状复发,可在 6 小时后进行第 3 次注射。在 24 小时内给药不可超过 3 次。在已完成的临床试验中,每个月的给药次数未超过 8 次。儿童患者本品的推荐剂量需要依据儿童和青少年(2-17 周岁)的体重确定,详见表 1。
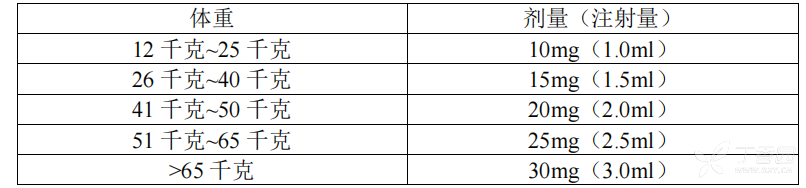
在已完成的临床试验中,遗传性血管水肿(HAE)发作时的给药次数未超过 1 次。对于不足 2 周岁或体重低于 12 千克的儿童不建议使用试验剂量方案,因为该药物对这一年龄阶段的儿童用药的安全性和有效性尚未确定。老年患者超过 65 周岁的患者资料不足。老年患者使用后会出现艾替班特全身暴露增加,这与本品的安全性方面的关系尚不可知。建议无需调整剂量。肝脏损伤肝损伤患者在治疗时不需要调整剂量。肾脏损伤肾损伤患者在治疗时不需要调整剂量。给药指导
推荐于腹部区域皮下注射本品。注射本品时应当缓慢注射。每瓶醋酸艾替班特注射液仅能使用一次。给药前应肉眼观测颗粒和变色。药物溶液应无色透明。如产品含颗粒或变色不要给药。消毒注射部位,皮下注射给药时间至少 30 秒。对于通过护理人员给药或自身注射给药,应当由在诊断和治疗遗传性血管水肿方面有丰富经验的医生来决定。对于从未注射过本品的患者,第一次注射治疗应当在医疗机构或在医师的指导下进行。在获得专业医疗人员的有关皮下注射的培训,并确认患者可安全、准确进行皮下注射后,成年人方可进行自身注射或通过护理人员注射本品。2-17 岁的儿童和青少年患者,需由经过专业医疗人员皮下注射培训的护理人员注射本品。

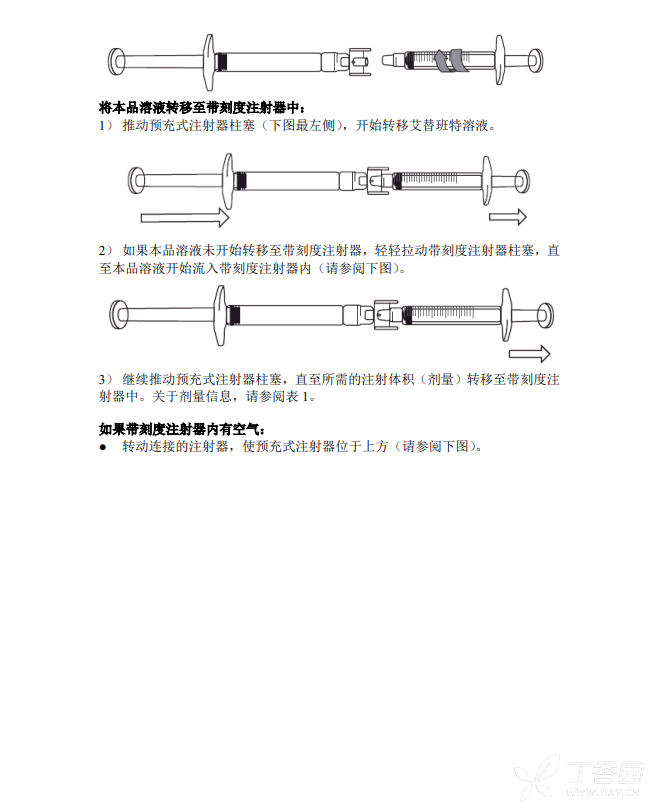
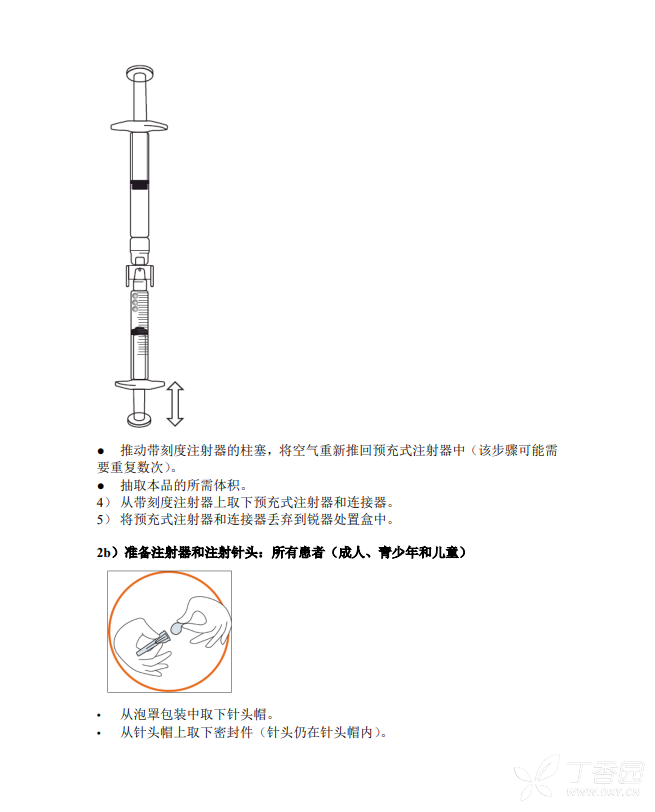
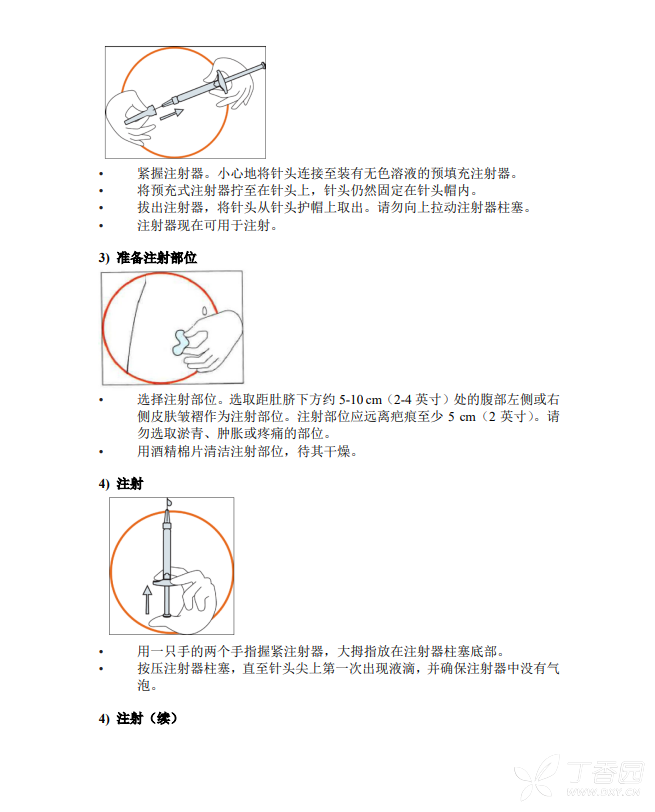

【临床药理】
艾替班特是缓激肽 B2 受体的竞争性拮抗剂,亲和力与缓激肽相似。遗传性血管水肿(HAE)是一种由 C1-酯酶抑制剂缺乏或功能障碍所致的遗传疾病,C1-酯酶抑制剂是凝血因子 XII/激肽释放酶蛋白水解级联反应(该反应导致缓激肽生成)的关键调节因子。缓激肽是一种血管舒张物质,被认为可引起 HAE 的典型症状,如局部肿胀、炎症和疼痛。艾替班特可抑制缓激肽与 B2 受体结合,从而治疗 HAE 急性发作时的临床症状。
【药理毒理】
遗传毒性:艾替班特 Ames 试验、中国仓鼠骨髓细胞染色体畸变试验、小鼠体内微核试验结果均为阴性。
生殖毒性:大鼠、犬每日皮下给予艾替班特,可导致卵巢、子宫、睾丸萎缩/变性,乳腺、前列腺出现不良反应。在大鼠中, ≥ 3 mg/kg[按 AUC 计,约为人体最大推荐剂量(MRHD)的 5 倍(男性)和 2 倍(女性)以上]可见睾丸萎缩、前列腺分泌减少、睾酮水平降低、黄体退化;雌鼠在 ≥ 10 mg/kg 剂量(按 AUC 计,约为女性 MRHD 的 6 倍以上)可见发育卵泡减少、乳腺雄性化和子宫萎缩。在犬中, ≥ 1 mg/kg(按 AUC 计,约为 MRHD 的 2 倍以上)可见精子计数减少、子宫萎缩;10 mg/kg[按 AUC 计,约为 MRHD 的 30 倍(男性)和 15 倍(女性)以上]可见睾丸和前列腺萎缩及睾酮水平降低,卵巢变小及发育卵泡数量减少。与每日给药出现的毒性相反,犬持续 9 个月每周 2 次给予艾替班特,未见卵巢、子宫、睾丸、乳腺和前列腺毒性,3 mg/kg 剂量下的 AUC 分别约为 MRHD 的 5 倍(男性)和 3 倍(女性)。雄犬每周 2 次给药未见对精子数量、睾丸的影响。雄性小鼠每日静脉给予艾替班特达 81 mg/kg(按体表面积计,约为 MRHD 的 5 倍以上),大鼠每日皮下给予艾替班特达 10 mg/kg(按 AUC 计,约为 MRHD 的 11 倍以上),均未见对生育力或生殖行为的影响。在大鼠生育力和早期胚胎发育毒性试验中,皮下注射给予艾替班特 10 mg/kg/d(按 AUC 计,为 MRHD 的 7 倍),可致胚胎着床前丢失增加。
在大鼠胚胎-胎仔发育毒性试验中,自妊娠第 7 天至 18 天皮下注射给予艾替班特达 25 mg/kg/d(按体表面积计,相当于 MRHD 的 2.7 倍),未见致畸作用或对胚胎、胎仔存活的影响。在兔胚胎-胎仔发育毒性试验中,自妊娠第 7 天至 18 天皮下注射给予艾替班特, ≥ 0.1 mg/kg(按体表面积计,约为 MRHD 的 0.025 倍以上)可致早产和流产; 10 mg/kg/d 剂量(按 AUC 计,约为 MRHD 的 13 倍)可见剂量依赖性的着床数和活胎数减少以及剂量依赖性的着床前丢失率增加;剂量高达 10 mg/kg/d,未见致畸作用。
在大鼠围产期发育毒性试验中,自妊娠第 6 天至产后第 20 天皮下注射给予艾替班特 1、3、10 mg/kg/d(按 AUC 计,分别相当于 MRHD 的 0.5 倍、2 倍、7 倍), ≥ 1 mg/kg/d 可见分娩延迟, ≥ 3 mg/kg/d 可见分娩延迟导致的母鼠死亡, ≥ 3 mg/kg/d 可见胎仔死亡及出生后 4 天幼仔死亡增加,10 mg/kg 剂量可见 F1 代翻正反射受损及毛发生长速度降低。皮下注射艾替班特后,可在母鼠乳汁中检测到原型药及代谢产物 M2。艾替班特对 F1 代的未见反应剂量为 1 mg/kg/d,未得到对 F0 代母鼠的未见反应剂量。致癌性:小鼠(每周 2 次)、大鼠(每日 1 次)连续 2 年皮下给予艾替班特 2 年,剂量分别达 15 mg/kg/d、6 mg/kg/d,未见致癌性,按照 AUC 计,分别约相当于最大推荐人体剂量(MRHD)暴露量的 10 倍、6 倍以上。幼龄动物毒性:大鼠于幼龄发育阶段(出生后 22 天至 70 天)每日皮下给予艾替班特,按体表面积计,在约 ≥ 1/3 MRHD 剂量下可延迟雄性生殖器官的性成熟(睾丸和附睾萎缩),在高于或约相当于 MRHD 剂量下可导致给药期末雄鼠的生育力和生殖能力受损,在约为 3 倍 MRHD 剂量下未见对雌鼠的影响。雄性幼龄大鼠的组织病理学改变与性成熟大鼠和犬中结果一致,这归因于对缓激肽 B2 受体的拮抗作用以及对促性腺激素的继发影响。以上发现的反应可能为艾替班特每日给药的结果,犬连续 9 个月每周给药 2 次未见睾丸毒性。其它毒性:
【药代动力学】
吸收皮下注射 30 mg 后,本品的绝对生物利用度约为 97%。健康受试者(N = 96)单次皮下注射艾替班特 30 mg 后,约 0.75 小时后检测到平均(±标准差)最大血药浓度(Cmax)为 974±280 ng/mL。30 mg 剂量单次给药后的平均浓度-时间曲线下面积(AUC0-∞)为 2165±568 ng·hr/mL,3 次 30 mg 剂量间隔 6 小时给药后未观察到艾替班特累积证据。分布
醋酸艾替班特分布容积(Vss)约为 20-25 L。血浆蛋白结合率为 44%。消除醋酸艾替班特主要通过代谢消除,少于 10% 的剂量作为原形药物经尿液消除。清除率约为 15-20 L/h,与剂量无关。终末血浆半衰期约为 1-2 小时。生物转化醋酸艾替班特经蛋白水解酶广泛代谢成无活性代谢产物,主要经尿液排泄。体外研究证实,醋酸艾替班特不经氧化代谢途径降解,也不是主要细胞色素 P450(CYP)同工酶(CYP 1A2、2A6、2B6、2C8、2C9、2C19、2D6、2E1 和 3A4)的抑制剂,而且也不是 CYP 1A2 和 3A4 的诱导剂。特殊人群年龄和性别在年轻(18 至 45 岁)和老年(超过 65 岁)健康男性和女性受试者中每 6 小时给予 30 mg 皮下剂量艾替班特、共给药三次的研究中,单次-剂量 30 mg 皮下给予艾替班特后,老年男性和女性与年轻男性和女性比较显示 AUC 分别较高接近 2 倍。但是,观察到性别匹配的老年和年轻受试者 Cmax 间只有较小差别(12-14%)。老年受试者较年轻受试者清除率低,故全身暴露较高。除了年龄效应也观察到性别对艾替班特药代动力学的影响。注意到艾替班特清除率与体重相关,较低体重者则艾替班特清除率较低。因此,相比男性,女性通常体重较低,艾替班特清除率值也较低,导致接近 2 倍高的全身暴露(AUC 和 Cmax)。尚未确定老年和较年轻患者及男性和女性患者间疗效和安全性差别。无需根据年龄和性别调整剂量。肝损害发现健康受试者(n = 8)和轻至中度(Child Pugh 评分 5 至 8)肝受损受试者(n = 8)以 0.15 mg/kg/天剂量连续静脉输注艾替班特超过三天后,药代动力学参数具有可比性。在另一研究中,严重肝受损受试者中(Child-Pugh 评分 7 至 15) 艾替班特清除率与健康受试者相似。对肝功能受损患者无需调整剂量。肾损害
因为艾替班特的肾清除是次要消除通路,预计肾受损不影响艾替班特的药代动力学,因此对艾替班特未进行正规的肾受损研究。10 例患有肝肾综合征的(GFR 30-60 mL/min)受试者艾替班特的清除率不依赖于肾功能,艾替班特或其代谢物血浆水平与正常肾功能受试者比较未显示任何可观察到的差别。肾功能受损患者无需调整剂量。种族单个种族药效的信息是有限的。已有的数据显示清除量在非白种人(n = 40)和白种人(n = 132)之间没有显著差异。儿童通过在 HGT-FIR-086 研究中儿童 HAE 患者给药,确定了艾替班特的药代动力学。单次皮下给药(0.4 mg/千克,最多 30 mg,达峰时间约为 30 分钟),终末半衰期约为 2 小时。给药至发作和没有发作的 HAE 患者,两者之间暴露未见显著差异。群体药代动力学模型中成人和儿童的数据显示艾替班特的清除率与体重有关,儿童 HAE 患者的体重越轻,清除率越低。基于根据体重给药的建模,儿童 HAE 患者艾替班特的预计暴露量低于成人 HAE 患者研究中观察到的暴露量。
【生产企业】
企业名称:Vetter Pharma-Fertigung GmbH & Co.KG
【上市许可持有人】
Takeda Pharmaceuticals International AG Ireland Branch

