首页 > 注射用重组人凝血因子VIII说明书
修改日期:2012年4月28日|2021年11月23日
注射用重组人凝血因子VIII说明书(Baxalta Manufacturing Sàrl)
请仔细阅读说明书并在医师指导下使用
- 【药品名称】
- 通用名称: 注射用重组人凝血因子VIII
处方药物
【成份】
本品为采用基因重组技术以中国仓鼠卵巢细胞生产的重组人凝血因子 VIII。
活性成分:重组人凝血因子 VIII。
冻干粉辅料:甘露醇、氯化钠、组氨酸、海藻糖、氯化钙、三羟甲基氨基甲烷、聚山梨醇酯 80、谷胱甘肽。
稀释液:灭菌注射用水。
【适应症】
本品适用于血友病 A(先天性凝血因子 VIII 缺乏)患者出血的治疗和预防。
本品不含具有药效作用剂量的 von Willebrand 因子,因此不适用于血管性血友病。
【规格】
250IU/瓶;500IU/瓶;1000IU/瓶;1500IU/瓶
【用法用量】
本品应在有治疗血友病经验的医生指导下使用。出现速发型超敏反应时,能立即获得复苏支持。
给药剂量:
使用本品替代治疗的剂量和持续时间取决于凝血因子 VIII 缺乏的严重程度、出血部位、范围以及患者的临床情况。
以国际单位 IU 标示本品重组人凝血因 VIII 的效价。血浆中凝血因子 VIII 活性以 IU 或者百分数(相对于正常人血浆)来表示。
1 个 IU 本品重组凝血因子 VIII 的活性等效于 1 mL 正常人血浆中的凝血因子 VIII。
按需治疗:
根据经验计算按需治疗所需剂量,即,给予每 kg 体重 1IU 的本品可以使血浆凝血因子 VIII 活性提高 2IU/dL。所需剂量按以下公式计算:
治疗所需本品剂量(IU) = 体重(kg) × 预期的因子 VIII 升高值(IU/dL 或%) × 0.5
当发生表 1 中所列出血事件时,相应时期因子 VIII 活性不应低于给定的血浆活性水平(IU/dL 或 %)。下表 1 可用于出血和外科手术时指导给药剂量。
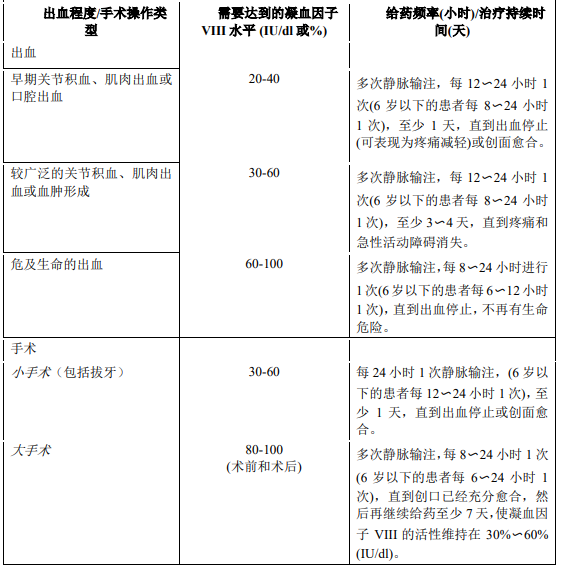
应根据个体对治疗的临床反应调整给药剂量和频率。在某些情况下(如出现低滴度抑制物),可能需要使用比上述公式计算所得结果更大的剂量。
在治疗期间,建议适当检测血浆凝血因子 VIII 水平以指导给药的剂量和重复注射的频率。尤其在实施大手术的情况下,必须通过测定血浆凝血因子 VIII 的活性来对替代治疗进行准确的监测。由于存在个体间差异,本品在不同患者体内的回收率和半衰期可能会不同。
预防用药:
对于严重血友病 A 患者出血的长期预防,常规剂量为每 kg 体重 20-40IU,给药间隔为 2-3 天。
儿童用药:
对于按需治疗,儿童患者(0-18 岁)的剂量与成年患者并无不同。对于 6 岁以下的患者,推荐采用 20-50IU 因子 VIII 每 kg 体重、每周 3-4 次进行预防性治疗。
给药方法:
本品应通过静脉给药。如为非专业医务人员给药,需要进行适当的培训。
给药速率的确定以使患者舒适为宜,最快不应超过 10 mL/分钟。
配制后,应为澄清、无色、不含异物的溶液,pH 为 6.7 至 7.3。
每次给药后,均应登记产品的名称及批号。给药前按照所附说明配制本品。
本品的使用说明
本品使用所附的冻干粉及 5 mL 灭菌注射用水配制后,即可经静脉给药。
应目检配制后溶液是否有任何异物和/或变色。不得使用浑浊、或有沉淀的溶液。
给药时必须使用带有鲁尔接头的注射器。同时,必须使用塑料注射器,因为本品中的蛋白质成分易与玻璃注射器的表面发生粘附。
- 本品配制后,应在 3 小时内使用。
- 本品配制后不得冷冻。
- 根据地方要求处置任何未使用的产品或废弃物。
【禁忌】
对本品活性成份或对任何辅料过敏/超敏,对小鼠或仓鼠蛋白有过敏/超敏反应者。
【注意事项】
- 超敏反应
- 因子 VIII 抑制物产生因子 VIII 中和抗体(抑制物)的产生是血友病 A 患者治疗中的已知并发症。这些抑制物通常是直接针对因子 VIII 促凝活性的 IgG,使用改良 Bethesda 法检测,单位为 Bethesda 单位(BU)/mL 血浆。产生因子 VIII 抑制物的患者可能表现为临床疗效不佳。在这种情况下,建议联系专门的血友病中心。产生抑制物的风险与暴露于因子 VIII 的程度以及其他遗传和环境因素有关,前 20 个暴露日内的风险最高,100 个暴露日以后极少产生抑制物。 已在之前治疗超过 100 暴露日且有抑制物产生史的患者中观察到在因子 VIII 产品替换使用后会重新出现抑制物的情况(低滴度)。因此,在改变治疗产品时,建议仔细监测所有患者的抑制物出现情况。 一般而言,应通过适当的临床观察和实验室检测,密切监测接受因子 VIII 治疗的患者的抑制物产生。若患者接受治疗后达不到预期的因子 VIII 血浆活性水平,或者在适当剂量下出血不受控制,应进行检测以确定是否存在因子 VIII 抑制物。在具有高滴度抑制物的患者中,因子 VIII 替代疗法可能无效,应考虑其他的治疗方法。这类患者的管理应在具有血友病和因子 VIII 抑制物治疗经验的医师指导下进行。
- 与导管有关的并发症
- 与辅料有关的考虑本品配制后每瓶含 0.45mmol 钠(10 mg),限钠饮食患者应予以考虑。强烈建议每次给患者使用本品时,记录本品名称和批号,以维持患者和该批次药品之间的联系。
- 由于缺乏相容性研究,本品不得与其他药用产品或溶剂混合使用。
- 本品对驾驶及操作机械的能力没有影响【对驾驶及操作机械的影响】。
【临床药理】
本品含重组凝血因子 VIII(辛凝血素α,它是一种与在人血浆中发现的因子 VIII 糖蛋白生物等效的糖蛋白。
因子 VIII/von Willebrand 复合物包括两种具有不同生理功能的分子(因子 VIII 和 von Willebrand 因子)。辛凝血素α是一种含有 2332 种氨基酸的糖蛋白,分子量约为 280kD。当输注给血友病患者时,辛凝血素α与患者循环中的内源性 von Willebrand 因子结合。活化的因子 VIII 作为活化的因子 IX 的辅助因子,加速因子 X 转化为活化的因子 X。活化的因子 X 使凝血酶原转化为凝血酶。凝血酶使纤维蛋白原转化为纤维蛋白,形成凝块。血友病 A 是一种性连锁染色体遗传性凝血障碍,由因子 VIII 活性水平降低引起,并导致大量血液流入关节、肌肉或内脏器官,可为自发性或由意外或外科创伤而引起。替代治疗可增加血浆因子 VIII 水平,从而暂时纠正因子 VIII 缺乏并纠正出血倾向。
【药理毒理】
单次给予小鼠、大鼠、兔和犬高于临床推荐剂量数倍的本品(根据体重),未见任何急性毒性或其它毒性反应。本品未进行重复给药研究,可参考本品相关产品(RECOMBINATE)及本品制剂缓冲液(FORMULATION BUFFERS)的毒性试验信息。RECOMBINATE 在犬 2 周毒性试验中,观察到贫血,活化部分凝血活酶时间(APTT)延长,白细胞计数下降,(rAHF,pdAHF 和 HAS)抗体生产。在 4 周毒性试验中,观察到(rAHF,pdAHF 和 HAS)抗体生成,未出现贫血和白细胞计数下降。本品制剂缓冲液在大鼠给药剂量达到最高剂量 40 mg/kg/day 时,连续 30 天,未观察到任何毒性反应。
【药代动力学】
所有应用本品的药代动力学研究,都是针对患有重度或中度血友病 A 的先前接受过治疗的患者(基线因子 VIII ≤ 2%)进行的。血浆样品的分析在中央实验室用一期凝固分析法进行。
总共 195 份符合重度血友病 A(基线因子 VIII ≤ 1%)的样本提供的药代动力学参数均包含在基于方案药代动力学的分析集中。对这些分析按婴儿(年龄 1 个月-2 岁)、儿童(年龄 2 岁-5 岁)、大龄儿童(年龄 5 岁-12 岁)、青少年(年龄 12 岁-18 岁)、成人(年龄 18 岁及以上)的分类方法进行分类,用于总结药代动力学参数。此处的年龄定义为接受 PK 输注的年龄。
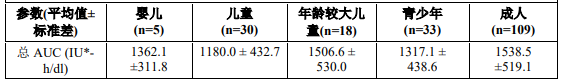
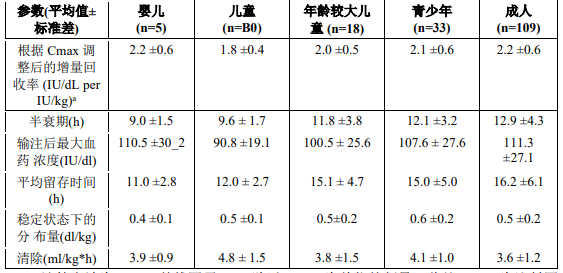
儿童患者使用本品的安全性和止血功效与成人患者相似。年幼儿童(低于 6 岁)校正后的体内因子 VIII 活性回收率和终末半衰期(t1/2)比成人约低 20%,可能是由于已知儿童患者每 kg 体重的血浆容积值较高。
目前尚无本品在既往未接受治疗患者(PUP)中的药代动力学数据。
在中国患者人群中进行了药代动力学相关临床研究,共分析了符合方案计划分析群的 22 名患者(6 名患者小于 6 岁,5 名患者为 6-12 岁,11 名患者为大于 12 岁),采用一期凝固分析法测定,并采用可用的群体药代动力学模型对比了本品在中国和非中国患者中的药代动力学特征,最终结果显示,使用本品的共 22 名中国患者未出现与非中国患者不同的药代动力学特征。
【生产企业】
企业名称:Baxalta Manufacturing Sàrl
【上市许可持有人】
Takeda Manufacturing Austria AG
