瑞莎珠单抗(Skyrizi)注射液详细说明书及处方信息
处方信息重点
近期重大变更
Skyrizi 注射液的适应症和用法
SKYRIZI 是一种白细胞介素 23 拮抗剂,用于治疗:
建议用量
斑块状银屑病和银屑病关节炎:
- 在第 0 周、第 4 周以及之后每 12 周通过皮下注射给药 150 毫克。(2.3、2.4 )
- 对于银屑病关节炎患者,SKYRIZI 可单独使用或与非生物抗风湿药物 (DMARD) 联合使用。( 2.4 )
克罗恩氏病:
- 建议诱导剂量为第 0 周、第 4 周和第 8 周静脉输注 600 mg,每次至少 1 小时。建议维持剂量为第 12 周皮下注射 180 mg 或 360 mg,此后每 8 周一次。使用最低有效剂量来维持治疗反应。(2.6)
溃疡性结肠炎:
- 建议诱导剂量为第 0 周、第 4 周和第 8 周静脉输注 1,200 mg,每次至少持续 2 小时。建议维持剂量为第 12 周皮下注射 180 mg 或 360 mg,此后每 8 周一次。使用最低有效剂量来维持治疗反应。(2.7)
禁忌症
- 对 risankizumab-rzaa 或任何辅料有严重过敏反应史的患者禁用 SKYRIZI ( 4 )
警告和注意事项
最常见的不良反应是:
- 斑块状银屑病和银屑病关节炎(≥ 1%):上呼吸道感染、头痛、疲劳、注射部位反应和癣感染。( 6.1 )
- 克罗恩病(>3%):
◦诱导:上呼吸道感染、头痛和关节痛。(6.1)
◦维持:关节痛、腹痛、注射部位反应、贫血、发热、背痛、关节病和泌尿道感染。(6.1)
- 溃疡性结肠炎 (≥3%):
◦诱导:关节痛。(6.1)
◦维持:关节痛、发热、注射部位反应和皮疹。(6.1)
如需报告疑似不良反应,请联系 AbbVie Inc. 电话 1-800-633-9110 或 FDA 电话 1-800-FDA-1088 或访问 www.fda.gov/medwatch。
修订日期:6/2024
完整处方信息
1. Skyrizi 注射液的适应症和用法
1.1 斑块状银屑病
SKYRIZI ®适用于治疗适合全身治疗或光疗的成人中度至重度斑块状银屑病。
1.2 银屑病关节炎
SKYRIZI 适用于治疗成人活动性银屑病关节炎。
1.3 克罗恩病
SKYRIZI 适用于治疗成人中度至重度活动性克罗恩病。
1.4 溃疡性结肠炎
SKYRIZI 适用于治疗成人中度至重度活动性溃疡性结肠炎。
2. Skyrizi 注射剂的用法用量
2.1 治疗开始前的程序
2.2 管理的一般考虑
- 给药前目视检查 SKYRIZI 是否有颗粒物和变色。溶液中可能含有少量半透明至白色颗粒。◦
SKYRIZI 150 mg/mL、180 mg/1.2 mL 和 360 mg/2.4 mL:无色至黄色、透明至微乳白色溶液。◦
SKYRIZI 90 mg/mL 和 600 mg/10 mL:无色至微黄色、透明至微乳白色溶液。◦
如果溶液含有大颗粒或浑浊或变色,请勿使用。
- 使用后丢弃。 请勿重复使用。
2.3 斑块状银屑病的推荐剂量
建议剂量为第 0 周、第 4 周以及之后每 12 周皮下注射 150 毫克。
2.4 银屑病关节炎的推荐剂量
建议剂量为第 0 周、第 4 周以及之后每 12 周皮下注射 150 毫克。
SKYRIZI 可单独使用,也可与非生物抗风湿药物 (DMARD) 联合使用。
2.5 制备和管理说明(斑块状银屑病和银屑病关节炎)
• 皮下注射 SKYRIZI 150 mg/mL 预充笔或预充注射器。
• 患者在接受皮下注射技术培训后可自行注射 SKYRIZI。向患者和/或护理人员提供适当的 SKYRIZI 皮下注射技术培训。
• 注射前,将装有 SKYRIZI 的纸盒从冰箱中取出,不要从纸盒中取出预充式注射笔或预充式注射器,让 SKYRIZI 在没有阳光直射的情况下达到室温(预充式注射笔为 30 至 90 分钟,预充式注射器为 15 至 30 分钟)。
• 请勿注射到皮肤敏感、淤青、红斑、硬化或受牛皮癣影响的区域。上臂、外臂的 SKYRIZI 注射只能由医疗保健专业人员或护理人员进行。
• 如果漏服一剂,请尽快补服。然后按常规时间恢复服药。
SKYRIZI“使用说明”包含有关 SKYRIZI 准备和管理的更详细说明[参见使用说明]。指导患者在给药前阅读使用说明。
2.6 克罗恩病的推荐剂量
成人患者:诱导
SKYRIZI 的推荐诱导剂量为第 0 周、第 4 周和第 8 周通过静脉输注至少一小时,每次 600 毫克。
成年患者:维护
SKYRIZI 的推荐维持剂量为第 12 周皮下注射 180 mg 或 360 mg,此后每 8 周一次。使用维持治疗反应所需的最低有效剂量。
2.7 溃疡性结肠炎的推荐剂量
成人患者:诱导
SKYRIZI 的推荐诱导剂量为 1,200 毫克,在第 0 周、第 4 周和第 8 周通过静脉输注至少两小时。
成年患者:维护
SKYRIZI 的推荐维持剂量为第 12 周皮下注射 180 mg 或 360 mg,此后每 8 周一次。使用维持治疗反应所需的最低有效剂量。
2.8 制备和管理说明(克罗恩病和溃疡性结肠炎)
静脉诱导给药方案:
1. SKYRIZI 静脉注射瓶旨在由医疗保健提供者使用无菌技术进行注射。
2. 静脉给药前,根据患者的适应症确定所需的 SKYRIZI 剂量和药瓶数量(见下表)。从药瓶中取出 10 mL SKYRIZI 溶液(600 mg/10 mL),注入含有 5% 葡萄糖注射液或 0.9% 氯化钠注射液(见下表1)的静脉输液袋或玻璃瓶中,最终浓度约为 1.2 mg/mL 至 6 mg/mL。丢弃药瓶中剩余的溶液。
指征 |
静脉诱导剂量 | SKYRIZI 600 mg/10 mL 瓶装数量 | 5%葡萄糖或 0.9%氯化钠注射液总量 |
| 克罗恩病 | 600 毫克 | 1 | 100 毫升、250 毫升、500 毫升 |
| 溃疡性结肠炎 | 1,200 毫克 | 2 | 250 毫升或 500 毫升 |
3. 对于 SKYRIZI 600 mg 剂量,至少静脉输注稀释溶液 1 小时;对于 SKYRIZI 1,200 mg 剂量,至少静脉输注 2 小时。如果冷藏保存,在开始静脉输注之前,让输液袋或玻璃瓶中的稀释 SKYRIZI 溶液升温至室温。
4. 请勿在同一静脉注射管道中与其他药物同时注射 SKYRIZI 稀释溶液。
小瓶和稀释溶液的处理和储存:
• 请勿摇晃输液袋或玻璃瓶中的药瓶或稀释溶液。
• 立即使用配制好的输液。如果不立即使用,请将稀释的 SKYRIZI 溶液冷藏并避光保存,保存温度为 36°F 至 46°F(2°C 至 8°C),最长 20 小时。
• 制备或从冷藏室取出后,稀释的 SKYRIZI 溶液可立即在最高 77°F (25°C) 的室温下保存(避免阳光照射)4 小时(从开始稀释到开始输注的累计时间)。
• 室温储存和管理期间可以暴露在室内光线下。
• 请勿冷冻。
皮下维持给药方案:
使用单剂量 180 毫克或 360 毫克预充药筒和随身注射器:
• SKYRIZI 应在医疗保健专业人员的指导和监督下使用。
• 患者在接受皮下注射技术培训后,可使用预装药筒的随身注射器自行注射 SKYRIZI。向患者和/或护理人员提供 SKYRIZI 皮下注射技术的适当培训。
• 在使用带有预充药筒的随身注射器之前,请将纸盒从冰箱中取出,并放置在远离阳光直射的环境中(45 至 90 分钟),让其达到室温,而无需从纸盒中取出预充药筒或随身注射器。
• 使用随身注射器在大腿或腹部皮下注射 SKYRIZI 180 mg/1.2 mL 或 SKYRIZI 360 mg/2.4 mL 预充药筒。
• 将预充式药筒插入体内注射器后 5 分钟内开始注射。
• 请勿注射到皮肤柔软、擦伤、发红、硬化或受任何病变影响的部位。
• 如果漏服一剂,请尽快补服。然后按常规时间恢复服药。
SKYRIZI“使用说明”包含有关 SKYRIZI 准备和管理的更详细说明[参见使用说明]。指导患者在给药前阅读使用说明。
使用 90 mg/mL 预充式注射器:
• 将每个 SKYRIZI 90 mg/mL 预充注射器皮下注射。
• 患者在接受皮下注射技术培训后可自行注射 SKYRIZI。向患者和/或护理人员提供适当的 SKYRIZI 皮下注射技术培训。
• 注射前,将纸盒从冰箱中取出,不要从纸盒中取出预充注射器,让 SKYRIZI 在没有阳光直射的情况下达到室温(15 至 30 分钟)。
• 使用 90 mg/mL 预充注射器按如下方式皮下注射 SKYRIZI 180 mg 或 SKYRIZI 360 mg:
◦ 使用 SKYRIZI 90 mg/mL 预充式注射器时,若要达到 180 mg 维持剂量,则需要两支 90 mg 预充式注射器。在不同的解剖位置(例如大腿或腹部)依次注射一支预充式注射器。
◦ 使用 SKYRIZI 90 mg/mL 预充式注射器时,若要达到 360 mg 维持剂量,则需要四支 90 mg 预充式注射器。在不同的解剖位置(例如大腿或腹部)依次注射预充式注射器。
• 请勿注射到皮肤敏感、淤青、红斑、硬化或受任何病变影响的区域。上臂、外臂的 SKYRIZI 给药只能由医疗保健专业人员或护理人员进行。
• 如果漏服一剂,请尽快补服。然后按常规时间恢复服药。
SKYRIZI“使用说明”包含有关 SKYRIZI 准备和管理的更详细说明[参见使用说明]。指导患者在给药前阅读使用说明。
3. 剂型和规格
皮下注射
SKYRIZI 笔
- 注射剂:每支单剂量预充笔中为无色至黄色、透明至微乳白色的溶液,浓度为 150 mg/mL。
SKYRIZI 预充式注射器
- 注射剂:每个单剂量预充注射器中为无色至微黄色、透明至微乳白色的溶液,浓度为 90 mg/mL。
- 注射剂:每个单剂量预充注射器中为无色至黄色、透明至微乳白色的溶液,浓度为 150 mg/mL。
SKYRIZI 预填充药筒,附带随附的注射器
- 注射剂:每个单剂量预充药筒中含有 180 mg/1.2 mL (150 mg/mL),为无色至黄色、透明至微乳白色的溶液,可与随身注射器一起使用。
- 注射剂:每个单剂量预充药筒中含有 360 mg/2.4 mL(150 mg/mL)的无色至黄色、透明至微乳白色的溶液,可与随身注射器一起使用。
静脉输液
SKYRIZI 小瓶
- 注射剂:每个单剂量小瓶中含有 600 mg/10 mL (60 mg/mL),为无色至微黄色、透明至微乳白色的溶液。
4.禁忌症
对 risankizumab-rzaa 或任何辅料有严重超敏反应史的患者禁用 SKYRIZI (见警告和注意事项(5.1))。
5. 警告和注意事项
5.1 超敏反应
据报道,使用 SKYRIZI 可能会引发严重的超敏反应,包括过敏反应。如果发生严重的超敏反应,请停止使用 SKYRIZI 并立即开始适当的治疗[请参阅不良反应 ( 6.1 )]。
5.2 感染
SKYRIZI 可能会增加感染风险[见不良反应(6.1)]。
对于任何有临床重要活动性感染的患者,在感染消退或得到充分治疗之前,不应开始使用 SKYRIZI 治疗。
对于患有慢性感染或有复发性感染史的患者,在开具 SKYRIZI 处方之前,请考虑风险和益处。指导患者如果出现临床重要感染的迹象或症状,应寻求医疗建议。如果患者出现此类感染或对标准疗法没有反应,请密切监测患者,在感染消退之前不要使用 SKYRIZI。
5.3 结核病
在开始使用 SKYRIZI 治疗之前,评估患者的结核病 (TB) 感染情况。在 3 期银屑病临床研究中,在研究期间同时接受 SKYRIZI 和适当结核病预防治疗的 72 名潜伏性结核病患者中,在 SKYRIZI 平均随访 61 周期间,无一人患上活动性结核病。两名服用异烟肼治疗潜伏性结核病的受试者因肝损伤而停止治疗。在 PsO-3 研究中,31 名未接受预防治疗的潜伏性结核病患者中,在 SKYRIZI 平均随访 55 周期间,无一人患上活动性结核病。对于有潜伏性或活动性结核病史且无法确认是否接受充分治疗的患者,应考虑在开始使用 SKYRIZI 之前进行抗结核病治疗。在 SKYRIZI 治疗期间和治疗后,监测患者是否出现活动性结核病的体征和症状。请勿给患有活动性结核病的患者服用 SKYRIZI。
5.4 炎症性肠病治疗中的肝毒性
据报道,一名克罗恩病患者(ALT 54x ULN、AST 30x ULN 和总胆红素 2.2x ULN)在接受两次 600 毫克静脉注射 SKYRIZI 后,出现了药物性肝损伤和皮疹的严重不良反应,需要住院治疗。肝功能检查异常在服用类固醇后得到解决。随后,SKYRIZI 停用。
对于克罗恩病和溃疡性结肠炎的治疗,应在治疗基线和诱导治疗期间评估肝酶和胆红素,治疗至少持续 12 周。随后根据常规患者管理进行监测。
对于有肝硬化迹象的患者,请考虑其他治疗方案。建议及时调查肝酶升高的原因,以识别药物性肝损伤的潜在病例。如果怀疑是药物性肝损伤,则应中断治疗,直到排除此诊断。指导患者如果出现提示肝功能障碍的症状,应立即就医。
5.5 疫苗接种
接受 SKYRIZI 治疗的患者应避免使用活疫苗。与免疫系统相互作用的药物可能会增加接种活疫苗后感染的风险。在开始使用 SKYRIZI 治疗之前,请根据现行免疫指南完成所有适合年龄的疫苗接种。目前尚无关于对活疫苗或非活性疫苗的反应的数据。
6. 不良反应/副作用
标签的其他章节讨论了以下不良反应:
6.1 临床试验经验
由于临床试验是在千差万别的条件下进行的,一种药物的临床试验中观察到的药物不良反应发生率不能直接与另一种药物的临床试验中的发生率进行比较,也可能无法反映实践中观察到的发生率。
斑块状银屑病
在斑块状银屑病的临床开发试验中,共有 2234 名受试者接受了 SKYRIZI 治疗。其中,1208 名银屑病患者接受 SKYRIZI 治疗至少一年。
我们汇总了安慰剂和阳性对照试验的数据,以评估 SKYRIZI 长达 16 周的安全性。总共有 1306 名受试者在 SKYRIZI 150 毫克组中接受了评估。
表 2 总结了在汇总临床试验 16 周对照期内,SKYRIZI 组发生率至少为 1% 且高于安慰剂组的药物不良反应。
| 药物不良反应 | SKYRIZI N = 1306 n (%) |
安慰剂N = 300 n (%) |
| 上呼吸道感染 | 170(13.0) | 29(9.7) |
| 头痛b | 46(3.5) | 6(2.0) |
| 疲劳 | 33(2.5) | 3(1.0) |
| 注射部位反应d | 19(1.5) | 3(1.0) |
| 癣感染 | 15(1.1) | 1(0.3) |
| a包括:呼吸道感染(病毒性、细菌性或未指明的感染)、鼻窦炎(包括急性)、鼻炎、鼻咽炎、咽炎(包括病毒性)、扁桃体炎 b包括:头痛、紧张性头痛、窦性头痛、颈源性头痛 c包括:疲劳、乏力 d包括:注射部位瘀斑、红斑、渗出、血肿、出血、感染、炎症、刺激、疼痛、瘙痒、反应、肿胀、温热 e包括:足癣、股癣、体癣、花斑癣、手癣、癣感染、甲真菌病 |
||
截至第 16 周,SKYRIZI 组中发生率 < 1% 但 > 0.1% 的受试者出现且发生率高于安慰剂组的药物不良反应包括毛囊炎和荨麻疹。
特定药物不良反应
感染
在前 16 周内,SKYRIZI 组有 22.1% 的患者(每 100 名受试者年发生 90.8 次感染),而安慰剂组有 14.7% 的患者(每 100 名受试者年发生 56.5 次感染),但并未导致停用 SKYRIZI。SKYRIZI 组和安慰剂组的严重感染发生率均≤0.4%。SKYRIZI 组的严重感染包括蜂窝织炎、骨髓炎、脓毒症和带状疱疹。在 PsO-1 和 PsO-2 研究中,截至第 52 周,感染发生率(每 100 名受试者年发生 73.9 次感染)与治疗前 16 周的感染率相似。
安全至第 52 周
截至第 52 周,未发现任何新的不良反应,不良反应发生率与治疗前 16 周的发生率相似。在此期间,导致研究终止的严重感染包括肺炎。
银屑病关节炎
接受 SKYRIZI 治疗的银屑病关节炎患者的整体安全性与斑块状银屑病患者的安全性基本一致。此外,在 3 期安慰剂对照试验中,SKYRIZI 组的肝脏事件发生率(5.4%,每 100 患者年 16.7 次事件)高于安慰剂组(3.9%,每 100 患者年 12.6 次事件)。其中,安慰剂组和 SKYRIZI 组中报告频率最高的最常见事件是 ALT 升高(安慰剂:n=12(1.7%);SKYRIZI:n=16(2.3%))、AST 升高(安慰剂:n=9(1.3%);SKYRIZI:n=13(1.8%))和 GGT 升高(安慰剂:n=5(0.7%);SKYRIZI:n=8(1.1%))。未报告严重肝脏事件。SKYRIZI 组 (n=16, 2.3%) 的超敏反应发生率高于安慰剂组 (n=9, 1.3%)。在 3 期安慰剂对照试验中,SKYRIZI 组报告的超敏反应发生率较高,包括皮疹(安慰剂:n=4 (0.6%); SKYRIZI:n=5 (0.7%))、过敏性鼻炎(安慰剂:n=1 (0.1%); SKYRIZI:n=2 (0.3%))和面部肿胀(安慰剂:n=0 (0.0%); SKYRIZI n=1 (0.1%))。在 2 期临床试验中,一名接受 SKYRIZI 治疗的受试者报告了一例过敏反应。
克罗恩病
在两项随机、双盲、安慰剂对照诱导研究 (CD-1、CD-2) 和一项随机、双盲、安慰剂对照剂量探索研究 (CD-4;NCT02031276) 中,对中度至重度活动性克罗恩病患者进行了长达 12 周的 SKYRIZI 研究。在一项随机、双盲、安慰剂对照维持研究 (CD-3) 中,对对诱导治疗有反应的受试者评估了长达 52 周的长期安全性[见临床研究 ( 14.3 )]。
在两项诱导研究(CD-1、CD-2)和剂量探索研究(CD-4)中,620 名受试者在第 0、4 和 8 周接受了 SKYRIZI 静脉诱导方案。在维持研究(CD-3)中,在研究 CD-1 和 CD-2 中,297 名受试者在接受 12 周 SKYRIZI 静脉诱导治疗后获得临床反应(定义为 CDAI 较基线降低至少 100 分),在第 12 周接受 180 mg 或 360 mg SKYRIZI 维持方案,之后每 8 周接受一次,最长持续 52 周。
表 3 显示了诱导研究中 > 3% 的受试者报告的不良反应,且其发生率高于安慰剂。
| 药物不良反应 | SKYRIZI 600 毫克静脉输液a N = 620 n (%) |
安慰剂N = 432 n (%) |
| 上呼吸道感染b | 66(10.6) | 40(9.3) |
| 头痛c | 41(6.6) | 24(5.6) |
| 关节痛 | 31(5.0) | 19(4.4) |
a在第 0 周、第 4 周和第 8 周静脉输注 600 毫克 SKYRIZI。b包括:流感样疾病、鼻咽炎、流感、咽炎、上呼吸道感染、病毒性上呼吸道感染、COVID-19、鼻塞、病毒性呼吸道感染、病毒性咽炎、扁桃体炎、上呼吸道炎症 c包括:头痛、紧张性头痛 |
||
表 4 显示了维持研究中 >3% 的受试者报告的不良反应,且其发生率高于安慰剂。
| 药物不良反应 | SKYRIZI 180 mg 皮下注射N = 155 n (%) |
SKYRIZI 360 毫克皮下注射N = 142 n (%) |
安慰剂N = 143 n (%) |
| 关节痛 | 13(8.4) | 13(9.2) | 12(8.4) |
| 腹痛b | 9(5.8) | 12(8.5) | 6(4.2) |
| 注射部位反应c,d | 7(4.5) | 8(5.6) | 4(2.8) |
| 贫血 | 7(4.5) | 7(4.9) | 6(4.2) |
| 发热 | 4(2.6) | 7(4.9) | 4(2.8) |
| 背痛 | 3(1.9) | 6(4.2) | 3(2.1) |
| 关节病 | 1(0.6) | 5(3.5) | 2(1.4) |
| 泌尿道感染 | 1(0.6) | 5(3.5) | 4(2.8) |
| a SKYRIZI 180 mg 或 360 mg,第 12 周,之后每 8 周一次,最多持续 52 周 b 包括:腹痛、上腹痛、下腹痛 c包括:注射部位皮疹、注射部位红斑、注射部位肿胀、注射部位荨麻疹、注射部位发热、注射部位疼痛、注射部位过敏、注射部位反应 d一些受试者多次发生注射部位反应。在此表中,在计算发生率时,每个受试者仅计算一次注射部位反应。 |
|||
特定药物不良反应
感染
在截至第 52 周的维持研究 (CD-3) 中,SKYRIZI 180 mg 组受试者的感染率为 32.3%(每 100 名受试者年 50.2 次事件),SKYRIZI 360 mg 组受试者的感染率为 36.6%(每 100 名受试者年 60.8 次事件),而 SKYRIZI 诱导后接受安慰剂的受试者的感染率为 36.4%(每 100 名受试者年 60.3 次事件)。SKYRIZI 180 mg 组受试者的严重感染率为 2.6%(每 100 名受试者年 2.7 次事件),SKYRIZI 360 mg 组受试者的严重感染率为 5.6%(每 100 名受试者年 7.4 次事件),而 SKYRIZI 诱导后接受安慰剂的受试者的严重感染率为 2.1%(每 100 名受试者年 2.4 次事件)。
血脂升高
在诱导试验 (CD-1、CD-2) 中,首先在开始使用 SKYRIZI 后 4 周评估脂质参数 (总胆固醇和低密度脂蛋白胆固醇 [LDL-C]) 的升高。在第 4 周观察到相对于基线的增加和相对于安慰剂的增加,并且保持稳定到第 12 周。SKYRIZI 诱导后,平均总胆固醇从基线增加 9.4 mg/dL 至第 12 周的平均绝对值 175.1 mg/dL。同样,平均 LDL-C 从基线增加 6.6 mg/dL 至第 12 周的平均绝对值 92.6 mg/dL。在 SKYRIZI 180 mg 维持治疗中,第 52 周平均 LDL-C 从基线增加 3.1 mg/dL 至平均绝对值 99.0 mg/dL,在 SKYRIZI 360 mg 维持治疗(CD-3)中,第 52 周平均 LDL-C 从基线增加 2.3 mg/dL 至平均绝对值 102.2 mg/dL。
溃疡性结肠炎
在一项随机、双盲、安慰剂对照诱导研究 (UC-1) 和一项随机、双盲、安慰剂对照剂量探索研究 (UC-3) 中,对中度至重度活动性溃疡性结肠炎患者进行了长达 12 周的 SKYRIZI 研究。在一项随机、双盲、安慰剂对照维持研究 (UC-2) 中,对对诱导治疗有反应的受试者进行了长达 52 周的长期安全性评估[见临床研究 ( 14.4 )]。
在诱导研究 (UC-1 和 UC-3) 中,712 例受试者在第 0、4 和 8 周接受了 SKYRIZI 1,200 mg 静脉诱导方案。在维持研究 (UC-2) 中,347 例达到临床反应的受试者(定义为 mMS 较基线下降 ≥2 分和 ≥30% 且 RBS 较基线下降 ≥1 或绝对 RBS ≤1)在第 12 周接受 SKYRIZI 180 mg 或 360 mg 皮下维持方案,此后每 8 周接受一次,最多持续 52 周。
在溃疡性结肠炎诱导研究(UC-1 和 UC-3)中,接受 SKYRIZI 治疗的受试者中报告的不良反应占≥3%,且发生率高于安慰剂,为关节痛(SKYRIZI 为 3% vs 安慰剂为 1%)。
表 5 显示了维持研究 (UC-2) 中接受 SKYRIZI 治疗的受试者中报告的不良反应,发生率≥3%,且高于安慰剂组。
| 药物不良反应 | SKYRIZI 180 mg 皮下注射N = 170 n (%) |
SKYRIZI 360 毫克皮下注射N = 177 n (%) |
安慰剂N = 173 n (%) |
| 关节痛 | 9(5.3) | 17(9.6) | 8(4.6) |
| 发热 | 8(4.7) | 7(4.0) | 6(3.5) |
| 注射部位反应b,c | 5(2.9) | 5(2.8) | 2(1.2) |
| 皮疹 | 7(4.1) | 1(0.6) | 3(1.7) |
| a SKYRIZI 180 mg 或 360 mg,第 12 周,之后每 8 周一次,最多持续 52 周 b包括:应用部位疼痛、注射部位红斑、注射部位疼痛、注射部位瘙痒、注射部位反应 c 一些受试者多次发生注射部位反应。在此表中,每个受试者仅计算一次注射部位反应以计算发生率。 d包括: 皮疹和黄斑皮疹 |
|||
特定药物不良反应
在诱导研究(UC-1 和 UC-3)和维持研究(UC-2)中,接受 SKYRIZI 治疗的 UC 受试者与接受安慰剂治疗的受试者相比,感染、严重感染和脂质升高的发生率与在诱导研究(CD-1、CD-2 和 CD-4)和维持研究(CD-3)中接受 SKYRIZI 治疗的 CD 受试者与接受安慰剂治疗的受试者相比,相似。
6.2 免疫原性
与所有治疗性蛋白质一样,该药物也有可能产生免疫原性。抗体形成的检测高度依赖于检测的灵敏度和特异性。此外,在检测中观察到的抗体(包括中和抗体)阳性发生率可能受到多种因素的影响,包括检测方法、样品处理、样品采集时间、伴随用药和潜在疾病。出于这些原因,将下文所述研究中的抗体发生率与其他研究或其他产品(包括其他 risankizumab 产品)中的抗体发生率进行比较可能会产生误导。
斑块状银屑病
到第 52 周,约 24% (263/1079) 接受 SKYRIZI 推荐剂量治疗的受试者产生了针对 risankizumab-rzaa 的抗体。在产生针对 risankizumab-rzaa 抗体的受试者中,约 57%(占所有接受 SKYRIZI 治疗的受试者的 14%)的抗体被归类为中和抗体。约 1% 接受 SKYRIZI 治疗的受试者的抗体滴度较高,与 risankizumab-rzaa 浓度较低和临床反应降低有关。
银屑病关节炎
到第 28 周,接受推荐剂量 SKYRIZI 治疗的受试者中约有 12.1% (79/652) 产生了 risankizumab-rzaa 抗体。产生 risankizumab-rzaa 抗体的受试者中均无被归类为中和的抗体。risankizumab-rzaa 抗体与银屑病关节炎临床反应的变化无关。与没有抗药抗体的受试者相比,有抗药抗体的受试者出现超敏反应 (6.3% (5/79)) 和注射部位反应 (2.5% (2/79)) 的比例更高 (3.8% (22/574) 出现超敏反应,0.7% (4/574) 出现注射部位反应)。这些超敏反应和注射部位反应均未导致停用 risankizumab-rzaa。
克罗恩病
到第 64 周,接受 SKYRIZI 诱导治疗后接受 360 毫克维持治疗的受试者中约有 3.4% (2/58) 产生了 risankizumab-rzaa 抗体。接受 SKYRIZI 诱导治疗后接受 180 毫克维持治疗的受试者 (0/57) 均未产生 risankizumab-rzaa 抗体。产生 risankizumab-rzaa 抗体的受试者中均无被归类为中和抗体。
溃疡性结肠炎
到第 64 周,接受 SKYRIZI 诱导治疗后接受 180 毫克或 360 毫克维持治疗的受试者中分别约有 8.9% (8/90) 或 4.4% (4/91) 产生了 risankizumab-rzaa 抗体。在产生 risankizumab-rzaa 抗体的受试者中,分别有 75%(占所有接受 SKYRIZI 诱导治疗后接受 180 毫克维持治疗的受试者的 6.7%)或 50%(占所有接受 SKYRIZI 诱导治疗后接受 360 毫克维持治疗的受试者的 2.2%)产生了被归类为中和的抗体。
6.3 上市后经验
在 SKYRIZI 获批后,已报告以下不良反应。由于这些反应是来自人数不确定的群体中自愿报告的,因此并不总是能够可靠地估计其发生频率或与 SKYRIZI 暴露之间的因果关系:
- 皮肤和皮下组织疾病:湿疹和皮疹
8. 特定人群的使用
8.1 怀孕
妊娠暴露登记
有一个妊娠暴露登记处,用于监测接受 SKYRIZI 治疗期间怀孕的女性的结果。鼓励患者拨打 1-877-302-2161 或访问 http://glowpregnancyregistry.com 进行登记。
风险摘要
目前有关孕妇使用 risankizumab 的药物警戒和临床试验数据不足以确定药物相关的重大出生缺陷、流产或其他不良母婴结局的风险。虽然没有关于 risankizumab-rzaa 的数据,但单克隆抗体可以主动转运穿过胎盘,而 SKYRIZI 可能会导致宫内暴露的婴儿出现免疫抑制。患有炎症性肠病的女性会出现不良妊娠结局(见临床注意事项)。
在一项强化产前和产后发育毒性研究中,怀孕的食蟹猴在器官形成期直至分娩期间每周皮下注射一次 5 或 50 mg/kg risankizumab-rzaa。在 50 mg/kg 剂量下,怀孕的食蟹猴胎儿/婴儿丢失率增加(见数据)。怀孕的食蟹猴接受 50 mg/kg 剂量时,其暴露量 (AUC) 约为人类接受最大推荐诱导剂量(1,200 mg)的 5 倍,为人类接受最大推荐维持剂量(360 mg)的 32 倍。在从出生到 6 个月大的幼猴中,未观察到与 risankizumab-rzaa 相关的对功能或免疫发育的影响。这些发现对人类的临床意义尚不清楚。
所有妊娠都有出生缺陷、流产或其他不良后果的背景风险。对于特定人群,重大出生缺陷和流产的背景风险尚不清楚。在美国普通人群中,临床确诊妊娠中重大出生缺陷和流产的背景风险估计分别为 2% 至 4% 和 15% 至 20%。
临床考虑
疾病相关的母体和胚胎/胎儿风险
已发表的数据表明,患有炎症性肠病的女性发生不良妊娠结局的风险与疾病活动性增加有关。不良妊娠结局包括早产(妊娠 37 周前)、低出生体重(低于 2,500 克)婴儿以及出生时小于胎龄儿。
胎儿/新生儿不良反应
随着妊娠的进展,内源性 IgG 抗体通过胎盘的运输量增加,并在妊娠晚期达到峰值。由于 risankizumab 可能会干扰对感染的免疫反应,因此在给宫内接触 SKYRIZI 的婴儿接种活疫苗之前,应考虑风险和益处。关于婴儿出生时血清中 risankizumab 的水平以及出生后 risankizumab 在婴儿血清中的持续持续时间的数据不足。虽然推迟宫内接触的婴儿活病毒免疫接种的具体时间范围尚不清楚,但由于该产品的半衰期,应考虑出生后至少 5 个月。
数据
动物数据
在食蟹猴中开展了一项强化的产前和产后发育毒性研究。从妊娠第 20 天至分娩,每周给怀孕的食蟹猴皮下注射 5 或 50 mg/kg risankizumab-rzaa,并在产后对食蟹猴(母猴和幼猴)进行 6 个月的监测。本研究未发现母猴毒性。治疗对生长发育、畸形、发育免疫毒理学或神经行为发育均无相关影响。然而,与载体对照组(19%)相比,risankizumab-rzaa 治疗组的胎儿/婴儿丢失率呈剂量依赖性增加(5 mg/kg 组和 50 mg/kg 组分别为 32% 和 43%)。 50 mg/kg 组胎儿/婴儿损失增加被认为与 risankizumab-rzaa 治疗有关。母体毒性的未观察到不良反应水平 (NOAEL) 确定为 50 mg/kg,发育毒性的 NOAEL 确定为 5 mg/kg。怀孕猴子中 5 mg/kg 剂量导致人类接受最大推荐诱导剂量 (1,200 mg) 的暴露量 (AUC) 约为 0.6 倍,人类接受最大推荐维持剂量 (360 mg) 的暴露量 (AUC) 约为 5 倍。在婴儿中,平均血清浓度以剂量依赖性方式增加,约为相应母体浓度的 17%-86%。产后,大多数成年雌性食蟹猴和所有接受 risankizumab-rzaa 治疗的婴儿在产后 91 天内血清中均有可测量的 risankizumab-rzaa 浓度。产后 180 天血清浓度低于可检测水平。
8.2 哺乳
风险摘要
目前尚无关于 risankizumab-rzaa 是否出现在人乳中、对母乳喂养婴儿的影响或对产奶量的影响的数据。内源性母体 IgG 和单克隆抗体会转移到人乳中。母乳喂养婴儿局部胃肠道暴露和有限的全身暴露对 risankizumab-rzaa 的影响尚不清楚。应考虑母乳喂养对发育和健康的益处,以及母亲对 SKYRIZI 的临床需求以及 SKYRIZI 或潜在母体疾病对母乳喂养婴儿的任何潜在不利影响。
8.4 儿科用途
SKYRIZI 对儿科患者的安全性和有效性尚未确定。
8.5 老年人使用
在接受 SKYRIZI 治疗的 6,862 名受试者中,共有 664 名受试者年龄在 65 岁或以上(243 名斑块状银屑病患者、246 名银屑病关节炎患者、72 名克罗恩病患者和 103 名溃疡性结肠炎患者),71 名受试者年龄在 75 岁或以上。
在每种适应症中,SKYRIZI 的临床研究均未纳入足够数量的 65 岁及以上受试者,因此无法确定他们的反应是否与年轻成年受试者不同。
基于年龄,未观察到 risankizumab-rzaa 药代动力学有临床意义上的差异[见临床药理学 ( 12.3 )]。
11. Skyrizi 注射剂说明
Risankizumab-rzaa 是一种白细胞介素 23 (IL-23) 拮抗剂,是一种人源化免疫球蛋白 G1 (IgG1) 单克隆抗体。Risankizumab-rzaa 采用重组 DNA 技术在中国仓鼠卵巢细胞中产生,分子量约为 149 kDa。
SKYRIZI(risankizumab-rzaa)注射剂 90 mg/mL 预充式注射器,用于皮下注射
每支 SKYRIZI 预充式注射器均含有无菌、无防腐剂、无色至微黄色、透明至微乳白色的溶液。每支注射器提供 90 毫克 risankizumab-rzaa,以及非活性成分聚山梨醇酯 20(0.2 毫克)、琥珀酸钠(0.63 毫克)、山梨醇(41 毫克)、琥珀酸(0.059 毫克)和注射用水(USP)。pH 值为 6.2。
SKYRIZI(risankizumab-rzaa)注射液 150 mg/mL 预充式注射器或预充式注射笔,用于皮下注射
每支 SKYRIZI 预充笔或预充注射器均含有无菌、无防腐剂、无色至黄色、透明至微乳白色的溶液。每支注射器和笔提供 150 毫克 risankizumab-rzaa 和非活性成分冰醋酸 (0.054 毫克)、聚山梨醇酯 20 (0.2 毫克)、醋酸钠 (0.75 毫克)、海藻糖 (63.33 毫克) 和注射用水 (USP)。pH 值为 5.7。
SKYRIZI (risankizumab-rzaa)注射液180 mg/ 1.2 mL (150 mg/ mL )预充式药筒,与随附的体内注射器配合使用,用于皮下注射
每个 SKYRIZI 预充式药筒均含有无菌、无防腐剂、无色至黄色、透明至微乳白色的溶液。每个药筒提供 180 毫克 risankizumab-rzaa,以及非活性成分冰醋酸 (0.065 毫克)、聚山梨醇酯 20 (0.24 毫克)、醋酸钠 (0.9 毫克)、海藻糖 (76 毫克) 和注射用水 (USP)。pH 值为 5.7。
SKYRIZI (risankizumab-rzaa)注射液360 mg/2.4 mL(150 mg/mL)预充式药筒,与随附的皮下注射器配合使用
每个 SKYRIZI 预充式药筒均含有无菌、无防腐剂、无色至黄色、透明至微乳白色的溶液。每个药筒提供 360 毫克 risankizumab-rzaa,以及非活性成分冰醋酸 (0.13 毫克)、聚山梨醇酯 20 (0.48 毫克)、醋酸钠 (1.8 毫克)、海藻糖 (152 毫克) 和注射用水 (USP)。pH 值为 5.7。
SKYRIZI 600 mg/10 mL(60 mg/mL)小瓶装,用于静脉输注
SKYRIZI(risankizumab-rzaa)注射剂 600 mg/10 mL(60 mg/mL)是一种无菌、无防腐剂、无色至微黄色、透明至微乳白色的溶液,装于 10 mL 单剂量小瓶中。
每瓶 10 毫升单剂量药瓶含有 600 毫克 risankizumab-rzaa,以及非活性成分冰醋酸(0.54 毫克)、聚山梨醇酯 20(2 毫克)、乙酸钠(7.5 毫克)、海藻糖(633.3 毫克)和注射用水(USP)。pH 值为 5.7。
12. Skyrizi 注射液-临床药理学
12.1 作用机制
Risankizumab-rzaa 是一种人源化 IgG1 单克隆抗体,可选择性结合人类 IL-23 细胞因子的 p19 亚基并抑制其与 IL-23 受体的相互作用。IL-23 是一种天然存在的细胞因子,参与炎症和免疫反应。
Risankizumab-rzaa 抑制促炎细胞因子和趋化因子的释放。
12.2 药效学
尚未对 risankizumab-rzaa 进行正式的药效学研究。
12.3 药代动力学
在健康受试者中,单剂量给药后,Risankizumab-rzaa 的血浆浓度按比例增加:皮下给药时从 18 毫克增加至 360 毫克(为最低推荐剂量的 0.12 至 2.4 倍,为最高推荐剂量的 0.05 至 1 倍);长达 3 小时的静脉输注给药时从 200 毫克增加至 1,800 毫克(为推荐剂量的 0.2 至 3 倍)。
在第 0 周、第 4 周以及之后每 12 周皮下注射 150 mg 治疗的斑块状银屑病患者中,估计稳态峰浓度 (C max ) 和谷浓度 (C trough ) 分别为 12 mcg/mL 和 2 mcg/mL。
采用相同的皮下给药方案,银屑病关节炎患者中的 risankizumab-rzaa 药代动力学与斑块状银屑病患者相似。
对于克罗恩氏病患者,在第 0、4 和 8 周接受 600 mg 静脉诱导剂量,在第 12 周以及之后每 8 周接受 180 mg 或 360 mg 皮下维持剂量治疗,在第 8-12 周期间,估计中位 C max和C谷分别为 156 mcg/mL 和 38.8 mcg/mL;在第 40-48 周期间,估计稳态中位 C max和 C谷分别为 180 mg 的 14.0 mcg/mL 和 4.1 mcg/mL,或 360 mg 的 28.0 mcg/mL 和 8.1 mcg/mL。
对于在第 0、4 和 8 周接受 1,200 mg 静脉诱导剂量治疗,然后在第 12 周以及之后每 8 周接受 180 mg 或 360 mg 皮下维持剂量治疗的溃疡性结肠炎受试者,在诱导期内(第 8-12 周),估计中位 C max和 C谷分别为 350 和 87.7 mcg/mL;在维持期内(第 40-48 周),估计稳态中位 C max 和 C谷分别为 180 mg 的 19.6 和 4.64 µg/mL 或 360 mg 的 39.2 mcg/mL 和 9.29 mcg/mL。
根据群体药代动力学分析,溃疡性结肠炎患者的 risankizumab-rzaa 药代动力学与克罗恩病患者的药代动力学大致相似。
吸收
risankizumab-rzaa 皮下注射后的绝对生物利用度估计为 74% 至 89%。在健康受试者中,单次皮下注射后,C max可在 3 至 14 天内达到。
分配
斑块状银屑病患者的估计稳态分布容积 (受试者间 CV%) 为 11.2 L (34%),克罗恩氏病患者的估计稳态分布容积为 7.68 L (64%)。
消除
对于斑块状银屑病和克罗恩病患者,估计全身清除率(受试者间 CV%)分别为 0.31 L/天(24%)和 0.30 L/天(34%),终末消除半衰期分别约为 28 天和 21 天。
risankizumab-rzaa 的代谢途径尚未明确。作为人源化 IgG1 单克隆抗体,risankizumab-rzaa 预计会以类似于内源性 IgG 的方式通过分解代谢途径降解为小肽和氨基酸。
特定人群
老年患者(≥65 岁)的Risankizumab-rzaa 暴露量(C谷值)与每种适应症的年轻成年患者相当。尚未进行任何研究来确定肾功能或肝功能损害对 Risankizumab-rzaa 药代动力学的影响。
体重
随着体重的增加,Risankizumab-rzaa 清除率和分布容积增加,而血浆浓度降低;然而,不建议根据体重调整剂量。
药物相互作用研究
细胞色素 P450 底物
在斑块状银屑病患者(risankizumab-rzaa 150 mg,于第 0、4、8 和 12 周皮下注射)和克罗恩病或溃疡性结肠炎患者(risankizumab-rzaa 1,800 mg,于第 0、4 和 8 周静脉注射,即分别为克罗恩病和溃疡性结肠炎推荐剂量的 3 倍和 1.5 倍)中,与 risankizumab-rzaa 同时使用时,未观察到咖啡因(CYP1A2 底物)、华法林(CYP2C9 底物)、奥美拉唑(CYP2C19 底物)、美托洛尔(CYP2D6 底物)或咪达唑仑(CYP3A 底物)暴露量的临床显著变化。
13. 非临床毒理学
13.1 致癌作用、致突变作用、生育能力受损
尚未对 SKYRIZI 进行致癌性和致突变性研究。
在性成熟雄性食蟹猴中,每周服用 50 mg/kg risankizumab-rzaa 26 周,其剂量 (AUC) 为人类接受最大推荐诱导剂量 (1,200 mg) 的暴露量 (AUC) 的 4 倍,为人类接受最大推荐维持剂量 (360 mg) 的暴露量的 39 倍,未观察到对雄性生育参数的影响。
14. 临床研究
14.1 斑块状银屑病
四项多中心、随机、双盲研究 [PsO-1(NCT02684370)、PsO-2(NCT02684357)、PsO-3(NCT02672852)和 PsO-4(NCT02694523)] 招募了 2,109 名 18 岁及以上的中度至重度斑块状银屑病受试者,其体表面积 (BSA) 受累面积≥10%,银屑病总体评估(斑块厚度/硬结、红斑和脱屑)的静态医生总体评估 (sPGA) 评分≥3(“中度”),严重程度等级为 0 至 4,银屑病面积和严重程度指数 (PASI) 评分≥12。
总体而言,受试者的基线 PASI 评分中值为 17.8,BSA 评分中值为 20%。19% 的受试者的基线 sPGA 评分为 4(“严重”)。共有 10% 的受试者有银屑病关节炎病史。
在所有研究中,38% 的受试者曾接受过光疗法,48% 的受试者曾接受过非生物全身疗法,42% 的受试者曾接受过用于治疗牛皮癣的生物疗法。
研究 PsO-1 和 PsO-2
在 PsO-1 和 PsO-2 研究中,共招募了 997 名受试者(其中 598 名受试者随机分配至 SKYRIZI 150 毫克组,200 名受试者随机分配至安慰剂组,199 名受试者分配至生物活性对照组)。受试者在第 0 周、第 4 周以及此后每 12 周接受治疗。
两项研究均评估了第 16 周与安慰剂相比对两个共同主要终点的反应:
- 获得 sPGA 分数 0(“清楚”)或 1(“几乎清楚”)的受试者比例
- 实现基线 PASI 至少降低 90%(PASI 90)的受试者比例
次要终点包括第 16 周达到 PASI 100、sPGA 0 和银屑病症状量表 (PSS) 0 的受试者比例。
结果如表6所示。
| 氧化钆-1 | 氧饱和度 | |||
| SKYRIZI (N=304) n (%) |
安慰剂(N=102)n(%) |
SKYRIZI (N=294) n (%) |
安慰剂(N=98) n (%) |
|
| sPGA 0 或 1(“清除或几乎清除” ) | 267(88) | 8(8) | 246(84) | 5 (5) |
| 90后 | 229(75) | 5 (5) | 220(75) | 2 (2) |
| sPGA 0(“清除”) | 112(37) | 2 (2) | 150(51) | 3 (3) |
| 100 岁之后 | 109(36) | 0 (0) | 149(51) | 2 (2) |
| a共同主要终点 | ||||
在第 16 周,通过检查年龄、性别、种族、体重、基线 PASI 评分和之前接受的全身或生物制剂治疗,未发现这些亚组对 SKYRIZI 的反应存在差异。
在第 52 周的 PsO-1 和 PsO-2 中,接受 SKYRIZI 的受试者达到 sPGA 0(分别为 58% 和 60%)、PASI 90(分别为 82% 和 81%)和 PASI 100(分别为 56% 和 60%)。
患者报告结果
两项研究均发现,与安慰剂组相比,第 16 周时疼痛、发红、瘙痒和灼热相关体征和症状均有所改善,这是通过 PSS 评估的。在 PsO-1 和 PsO-2 中,第 16 周时约有 30% 的 SKYRIZI 组受试者达到 PSS 0(“无”),而安慰剂组受试者中只有 1%。
研究PsO-3
PsO-3 研究招募了 507 名受试者(其中 407 名随机接受 SKYRIZI 150 毫克治疗,100 名接受安慰剂治疗)。受试者在第 0 周、第 4 周以及此后每 12 周接受治疗。
在第 16 周,SKYRIZI 在 sPGA 0 或 1(84% SKYRIZI 和 7% 安慰剂)和 PASI 90(73% SKYRIZI 和 2% 安慰剂)这两项共同主要终点上均优于安慰剂。第 16 周 SKYRIZI 和安慰剂的各自缓解率分别为:sPGA 0(46% SKYRIZI 和 1% 安慰剂);PASI 100(47% SKYRIZI 和 1% 安慰剂);和 PASI 75(89% SKYRIZI 和 8% 安慰剂)。
维持和持久的反应
在 PsO-1 和 PsO-2 中,在接受 SKYRIZI 治疗并在第 16 周达到 PASI 100 的受试者中,80% (206/258) 继续服用 SKYRIZI 的受试者在第 52 周达到 PASI 100。对于第 16 周对 PASI 90 有反应的受试者,88% (398/450) 的受试者在第 52 周达到 PASI 90。
在 PsO-3 中,最初服用 SKYRIZI 且在第 28 周时 sPGA 为 0 或 1 的受试者被重新随机分配,每 12 周继续服用 SKYRIZI 或停止治疗。在第 52 周,重新随机分配继续使用 SKYRIZI 治疗的受试者中有 87% (97/111) 的 sPGA 为 0 或 1,而重新随机分配停止使用 SKYRIZI 的受试者中有 61% (138/225) 的 sPGA 为 0 或 1。
14.2 银屑病关节炎
在两项随机、双盲、安慰剂对照研究中,对 1407 名 18 岁及以上患有活动性银屑病关节炎 (PsA) 的受试者(PsA-1 [NCT03675308] 中 964 名,PsA-2 [NCT03671148] 中 443 名)评估了 SKYRIZI 的安全性和有效性。
这些研究中的受试者根据银屑病关节炎分类标准 (CASPAR) 诊断患有 PsA 至少 6 个月,基线时 PsA 的中位持续时间为 4.9 年,≥ 5 个疼痛关节和≥ 5 个肿胀关节,以及基线时患有活动性斑块状银屑病或银屑病指甲疾病。关于基线临床表现,55.9% 的受试者 BSA ≥3% 且患有活动性斑块状银屑病;63.4% 和 27.9% 的受试者分别患有肌腱炎和指炎。在进一步评估银屑病指甲疾病的 PsA-1 中,67.3% 患有银屑病指甲疾病。
在 PsA-1 中,所有受试者之前均对非生物 DMARD 疗法反应不足或不耐受,且未接受过生物治疗。在 PsA-2 中,53.5% 的受试者之前对非生物 DMARD 疗法反应不足或不耐受,46.5% 的受试者之前对生物治疗反应不足或不耐受。
在两项研究中,受试者在第 0、4 和 16 周随机接受 SKYRIZI 150 毫克或安慰剂治疗。从第 28 周开始,所有受试者每 12 周接受一次 SKYRIZI 治疗。两项研究都包括长期延长,最长可达 204 周。关于合并用药,59.6% 的受试者正在接受甲氨蝶呤 (MTX) 治疗,11.6% 的受试者正在接受除 MTX 以外的非生物 DMARD 治疗,28.9% 的受试者正在接受 SKYRIZI 单药治疗。
对于这两项研究来说,主要终点是第 24 周达到美国风湿病学会 (ACR) 20 反应的受试者比例。
临床反应
在两项研究中,与第 24 周的安慰剂相比,SKYRIZI 治疗使疾病活动度指标显著改善。主要疗效结果见表 7和表8 。
在这两项研究中,无论同时使用非生物 DMARD、之前使用的非生物 DMARD 数量、年龄、性别、种族和 BMI 如何,均观察到类似的反应。在 PsA-2 中,无论之前是否接受过生物治疗,均观察到反应。
| 端点 | 安慰剂 N=481 反应率 |
SKYRIZI N=483 响应率 |
与安慰剂的差异 (95% 可信区间) |
| ACR20 反应* | |||
| 第 16 周 | 33.4% | 56.3 % | 23.1% (16.8, 29.4) |
| 第 24 周 | 33.5% | 57.3 % | 24.0% (18.0, 30.0) |
| ACR50 响应* | |||
| 第 16 周 | 11.1% | 26.4% | 15.4% (10.6, 20.2) |
| 第 24 周 | 11.3% | 33.4 % | 22.2% (17.3, 27.2) |
| ACR70 响应* | |||
| 第 16 周 | 2.7% | 11.8% | 9.2% (6.1, 12.4) |
| 第 24 周 | 4.7% | 15.3% | 10.5%(6.9, 14.2) |
| a. 多重对照 p≤0.001,SKYRIZI 与安慰剂比较。 *A 受试者在开始使用救援药物或同时使用 PsA 药物后被视为无反应者,这可能会对疗效评估产生重大影响。 |
|||
| 端点 | 安慰剂 N=219 反应率 |
SKYRIZI N=224 响应率 |
与安慰剂的差异(95% 可信区间) |
| ACR20 反应* | |||
| 第 16 周 | 25.3% | 48.3 % | 22.6% (13.9, 31.2) |
| 第 24 周 | 26.5% | 51.3 % | 24.5% (15.9, 33.0) |
| ACR50 响应* | |||
| 第 16 周 | 6.8% | 20.3% | 13.5% (7.3, 19.7) |
| 第 24 周 | 9.3% | 26.3% | 16.6% (9.7, 23.6) |
| ACR70 响应* | |||
| 第 16 周 | 3.4% | 11.2% | 7.8% (3.0, 12.6) |
| 第 24 周 | 5.9% | 12.0% | 6.0% (0.8, 11.3) |
| a. 多重对照 p≤0.001,SKYRIZI 与安慰剂比较。 *A 受试者在开始使用救援药物或同时使用 PsA 药物后被视为无反应者,这可能会对疗效评估产生重大影响。 |
|||
图 1 显示了 PsA-1 研究中截至第 24 周达到 ACR20 反应的受试者百分比。
图 1. PsA-1 研究中截至第 24 周达到 ACR20 反应的受试者百分比
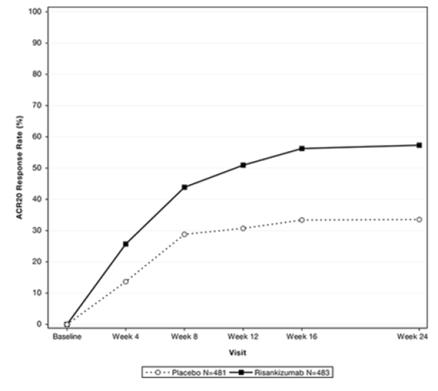
两项研究的ACR反应标准各组成部分的结果如表9所示。
| 银屑病A-1 | 银屑病-2 | |||
| 安慰剂 (N=481) 平均值 (SD) |
SKYRIZI (N=483) 平均值 (SD) |
安慰剂 (N=219) 平均值 (SD) |
SKYRIZI (N=224) 平均值 (SD) |
|
| 肿胀关节数 (0-66) | ||||
| 基线 | 12.2(8.0) | 12.1(7.8) | 13.6(9.0) | 13.0(8.7) |
| 第 16 周的平均变化 | -5.5(7.0) | -7.7 (7.2) | -5.4(8.5) | -8.0(7.4) |
| 第 24 周的平均变化 | -6.7 (7.2) | -8.7 (7.2) | -6.5(7.8) | -9.1(7.6) |
| 疼痛关节数 (0-68) | ||||
| 基线 | 20.5(12.8) | 20.8(14.0) | 22.3(13.8) | 22.8(14.9) |
| 第 16 周的平均变化 | -6.3 (11.1) | -10.7 (11.4) | -6.0 (13.1) | -11.3(13.0) |
| 第 24 周的平均变化 | -7.9(10.7) | -12.0(12.3) | -8.3 (11.3) | -13.0 (12.5) |
| 患者对疼痛的评估 | ||||
| 基线 | 57.1(22.6) | 57.1(22.6) | 57.0(23.1) | 55.0(23.5) |
| 第 16 周的平均变化 | -8.6 (23.7) | -18.4 (26.3) | -5.7 (22.7) | -14.4 (26.4) |
| 第 24 周的平均变化 | -10.9(25.4) | -21.4(26.5) | -8.7 (25.3) | -15.3(26.5) |
| 患者整体评估 | ||||
| 基线 | 57.4(22.1) | 57.9(21.7) | 56.2(23.0) | 56.2(21.8) |
| 第 16 周的平均变化 | -10.2(23.9) | -19.4(25.7) | -4.9 (23.6) | -17.0(27.1) |
| 第 24 周的平均变化 | -11.1 (25.1) | -22.6(26.9) | -8.7 (25.4) | -17.7 (27.7) |
| 医生整体评估 | ||||
| 基线 | 62.4(17.0) | 61.3(17.6) | 60.7(16.4) | 63.0(17.0) |
| 第 16 周的平均变化 | -18.3(22.5) | -31.1 (23.4) | -19.0(23.3) | -32.7(24.7) |
| 第 24 周的平均变化 | -22.2 (22.8) | -34.8(23.2) | -21.3 (25.2) | -35.5(25.6) |
| 健康评估问卷-残疾指数 (HAQ-DI) b | ||||
| 基线 | 1.2(0.7) | 1.2(0.7) | 1.1(0.6) | 1.1(0.6) |
| 第 16 周的平均变化 | -0.1(0.5) | -0.3(0.5) | -0.1(0.5) | -0.2(0.5) |
| 第 24 周的平均变化 | -0.1(0.5) | -0.3(0.5) | -0.1(0.4) | -0.2(0.5) |
| 高敏C反应蛋白(hs-CRP)mg/L | ||||
| 基线 | 11.3(14.1) | 11.9(15.9) | 8.2(17.1) | 7.4(10.9) |
| 第 16 周的平均变化 | -0.3(14.7) | -4.8 (14.2) | -0.1(6.8) | -2.1(7.5) |
| 第 24 周的平均变化 | -0.2(11.7) | -4.3(12.8) | -0.5(14.5) | -1.8 (13.4) |
| SD= 标准偏差。a . 根据视觉模拟量表 (100 mm) 进行评估,左端表示“无痛”(用于患者对疼痛的评估)、“非常好”(用于患者整体评估) 或“无关节炎活动”(用于医生整体评估),右端表示“最严重的疼痛”(用于患者对疼痛的评估)、“差”(用于患者整体评估) 或“极度活跃的关节炎”(用于医生整体评估)。b . 健康评估问卷的残疾指数;0 = 没有困难至 3 = 无法执行,测量患者执行以下活动的能力:穿衣、起身、进食、行走、卫生、伸手、抓握和日常生活活动。 |
||||
使用 SKYRIZI 治疗可改善患有指炎或肌腱炎的患者的指炎和肌腱炎。
在接受 SKYRIZI 治疗的共存斑块状银屑病患者中,与安慰剂相比,通过第 24 周的银屑病面积严重程度指数 (PASI 90) 测量,银屑病的皮肤病变随着治疗而改善。
身体机能
在两项研究中,与安慰剂组相比,接受 SKYRIZI 治疗的患者在第 24 周通过 HAQ-DI 评估的身体功能较基线有统计学显著改善(表 7)。第 24 周 HAQ-DI 与基线变化的平均差异(95% CI)在 PsA-1 研究中为 -0.20(-0.26,-0.14),在 PsA-2 研究中为 -0.16(-0.26,-0.07)。
在两项研究中,与第 24 周的安慰剂组相比,SKYRIZI 组中有更大比例的受试者的 HAQ-DI 评分较基线降低至少 0.35。
其他健康相关结果
两项研究均采用 36 项简明健康调查表 (SF-36 V2) 评估总体健康状况。采用慢性疾病治疗疲劳功能评估量表 (FACIT-Fatigue) 评估疲劳程度。
在两项研究中,第 24 周时,与接受安慰剂治疗的受试者相比,接受 SKYRIZI 治疗的受试者的 SF-36 身体成分总结分数有所改善。在两项研究中,第 24 周时,与接受安慰剂治疗的受试者相比,接受 SKYRIZI 治疗的受试者的身体机能、身体角色、身体疼痛、一般健康、活力、社会功能、心理健康、角色情绪领域分数和心理成分总结分数也有数值改善。在两项研究中,第 24 周时,与接受安慰剂治疗的受试者相比,接受 SKYRIZI 治疗的受试者的 FACIT-疲劳分数有所改善。
14.3 克罗恩病
诱导试验(研究 CD-1 和 CD-2)
在两项为期 12 周的诱导研究(CD-1;NCT03105128 和 CD-2;NCT03104413)中,中度至重度活动性克罗恩病患者在第 0 周、第 4 周和第 8 周随机接受 SKYRIZI 600 mg、SKYRIZI 1,200 mg 或安慰剂静脉输注。中度至重度活动性 CD 定义为克罗恩病活动指数 (CDAI) 为 220 至 450 且克罗恩病简易内镜评分 (SES-CD) ≥6(或孤立性回肠疾病为 ≥4)。入选受试者对口服氨基水杨酸盐、皮质类固醇、免疫抑制剂和/或生物疗法反应不足、反应丧失或不耐受。
基线时,CD-1 和 CD-2 的中位 CDAI 分别为 307(范围:76 – 634)和 307(范围:72 – 651),中位 SES-CD 分别为 12(范围:4 – 45)和 13(范围:4 – 40)。在 CD-1 中,58% (491/850) 的受试者对一种或多种生物疗法治疗失败或不耐受(先前的生物疗法失败)。CD-2 中的所有受试者均有先前的生物疗法失败。基线时,CD-1 和 CD-2 中分别有 30% 和 34% 的患者正在接受皮质类固醇治疗,24% 和 23% 的患者正在接受免疫调节剂(硫唑嘌呤、6-巯基嘌呤、甲氨蝶呤),31% 和 19% 的患者正在接受氨基水杨酸盐治疗。在 CD-1 和 CD-2 合并中,中位年龄为 36 岁(范围从 16 岁到 80 岁),81% (1145/1419) 的受试者为白种人,53% (753/1419) 为男性。
在 CD-1 和 CD-2 中,共同主要终点是第 12 周的临床缓解和内镜反应。次要终点包括临床反应和内镜缓解(见表10和表 11)。SKYRIZI 1,200 mg 剂量未显示出比 600 mg 剂量更多的治疗益处,因此不是推荐的治疗方案[见剂量和给药(2.6)]。
| 端点 | 安慰剂 |
SKYRIZI 600 毫克静脉输液 |
治疗 差异b (95% 可信区间) |
| 临床缓解c,d | |||
| 总人口 | 人数=175 25% |
人数=336 45% |
21%和 (12%, 29%) |
| 先前的生物学失败f | 样本量:97 26% |
样本量:195 42% |
|
| 无既往生物学失败 | 人数=78 23% |
人数=141 49% |
|
| 内镜反应c, g | |||
| 总人口 | 人数=175 12% |
人数=336 40% |
28%和 (21%, 35%) |
| 先前的生物学失败f | 人数=97 11% |
样本量:195 33% |
|
| 无既往生物学失败 | 人数=78 13% |
数量=141 50% |
|
| 临床反应 | |||
| 总人口 | 人数=175 37% |
人数=336 60% |
23%和 (14%, 32%) |
| 先前的生物学失败f | 人数=97 34% |
样本量:195 58% |
|
| 无既往生物学失败 | 人数=78 40% |
人数=141 62% |
|
| 内镜缓解i | |||
| 总人口 | 人数=175 9% |
人数=336 24% |
15%和 (9%,21%) |
| 先前的生物学失败f | 样本量:97 5% |
人数=195 18% |
|
| 无既往生物学失败 | 人数=78 14% |
人数=141 32% |
|
| a. 在第 0 周、第 4 周和第 8 周以静脉输注方式给予 600 毫克 SKYRIZI b. 基于 Cochran-Mantel-Haenszel 方法调整后的治疗差异(95% CI),并根据随机分层因素进行调整 c. 共同主要终点 d. CDAI <150 e. p <0.001 f. 先前的生物疗法失败包括对一种或多种 CD 生物疗法的反应不足、失去反应或不耐受 g. 根据中心读数,SES-CD 较基线下降 > 50%,或对于基线评分为 4 且患有孤立性回肠疾病的受试者, 下降至少 2 分 h. CDAI 较基线下降 ≥ 100 分 i. 根据中心读数,SES-CD ≤ 4,且较基线至少下降 2 分,且没有单个子评分大于 1 |
|||
| 端点 | 安慰剂 N=187 |
SKYRIZI 600 毫克静脉输注b N=191 |
治疗 差异c (95% 可信区间) |
| 临床缓解d, e | 20% | 42% | 22% ( 13%,31%) |
| 内镜反应d,g | 11% | 29% | 18%回升 (10%,25%) |
| 临床反应 | 30% | 60% | 29% ( 20%,39%) |
| 内镜缓解i | 4% | 19% | 15% ( 9%,21%) |
| a. 参加 CD-2 的所有受试者均曾出现过生物学失败。先前的生物学失败包括对一种或多种 CD 生物治疗的反应不足、反应丧失或不耐受 b. 在第 0 周、第 4 周和第 8 周静脉输注 600 毫克 SKYRIZI c. 基于 Cochran-Mantel-Haenszel 方法调整后的治疗差异(95% CI),并根据随机分层因素进行调整 d. 共同主要终点 e. CDAI 评分 <150 f. p < 0.001 g. 根据中心读数,SES-CD 较基线下降 > 50%,或对于基线评分为 4 且患有孤立性回肠疾病的受试者,下降至少 2 分 h. CDAI 较基线下降 ≥ 100 分 i. 根据中心读数,SES-CD ≤ 4,且与基线相比至少下降 2 分,且没有单个子评分大于 1 |
|||
与安慰剂相比,接受 SKYRIZI 600 mg 诱导方案治疗的受试者中,更大比例的受试者早在第 4 周就出现了基于 CDAI 的临床反应和临床缓解。
第 12 周时,与接受安慰剂治疗的受试者相比,接受 SKYRIZI 600 毫克诱导方案治疗的受试者中,排便频率和腹痛减少的比例更高。
学习 CD-3
维持研究 CD-3 评估了 382 名受试者,这些受试者在研究 CD-1 和 CD-2 中接受静脉注射 SKYRIZI 诱导治疗 12 周后,达到临床反应,定义为 CDAI 较基线至少降低 100 分。受试者在第 12 周随机接受 SKYRIZI 180 毫克或 SKYRIZI 360 毫克或安慰剂维持治疗方案,此后每 8 周接受一次,最多再接受 52 周。
CD-3 中的共同主要终点是第 52 周的临床缓解和内镜反应(见表12)。
| 端点 | 安慰剂 |
SKYRIZI 180 mg 皮下注射b |
SKYRIZI 360 毫克皮下注射c |
与安慰剂组相比的治疗差异(95% CI ) |
||
| SKYRIZI 180 毫克 |
SKYRIZI 360 毫克 |
|||||
| 临床缓解e,f | ||||||
| 总人口 | 人数=130 46% |
人数=135 61% |
人数=117 57% |
17%克 (6%,28%) |
14%克 (3%,26%) |
|
| 既往生物失败h | 数量=99 40% |
人数=95 56% |
人数=83 51% |
|||
| 无既往生物学失败 | 人数=31 65% |
人数=40 75% |
人数=34 71% |
|||
| 内镜反应e,i | ||||||
| 总人口 | 人数=130 22% |
人数=135 50% |
人数=117 48% |
30%克 (20%,39%) |
31%克 (21%,41%) |
|
| 既往生物失败h | 数量=99 21% |
人数=95 44% |
人数=83 44% |
|||
| 无既往生物学失败 | 人数=31 23% |
人数=40 65% |
人数=34 59% |
|||
| a. 安慰剂组由对 SKYRIZI 有反应的患者组成,并在维持治疗开始时随机接受安慰剂治疗。 b. 第 12 周服用 SKYRIZI 180 毫克,之后每 8 周服用一次,最多服用 52 周 c. 第 12 周服用 SKYRIZI 360 毫克,之后每 8 周服用一次,最多服用 52 周 d. 使用 Cochran-Mantel-Haenszel 方法计算的调整后治疗差异和 95% CI 已根据随机分层因素进行调整 e. 共同主要终点 f. CDAI <150 g. p <0.05 h. 先前的生物疗法失败包括对一种或多种 CD 生物疗法的反应不足、失去反应或不耐受 i. 根据中心读数,SES-CD 较基线下降 > 50%,或对于基线评分为 4 且患有孤立性回肠疾病的受试者,下降至少 2 分 |
||||||
在第 52 周,接受 SKYRIZI 180 mg 维持方案治疗的受试者中 33% (44/135) 观察到内镜缓解,接受 SKYRIZI 360 mg 维持方案治疗的受试者中 41% (48/117) 观察到内镜缓解,而接受安慰剂治疗的受试者中这一比例为 13% (17/130)。在预先指定的多重检验程序下,该终点无统计学意义。
14.4 溃疡性结肠炎
诱导试验(研究 UC-1)
在为期 12 周的诱导研究 (UC-1; NCT03398148) 中,966 名中度至重度活动性溃疡性结肠炎受试者随机分配,在第 0 周、第 4 周和第 8 周接受 SKYRIZI 1,200 毫克或安慰剂静脉输注。疾病活动性通过改良的 Mayo 评分 (mMS) 评估,该评分由 3 个部分组成 (0-9),包含以下子评分(每个子评分 0 到 3):大便频率 (SFS)、直肠出血 (RBS) 和集中读取内窥镜评分 (ES) 的发现。ES 为 2 的定义为明显红斑、缺乏血管模式、任何易碎性和/或糜烂;ES 为 3 的定义为自发性出血和溃疡。入选受试者的 mMS 在 5 到 9 之间,ES 为 2 或 3。入选受试者是对口服氨基水杨酸盐、皮质类固醇、免疫调节剂、生物制剂、Janus 激酶抑制剂 (JAKi) 和/或鞘氨醇-1-磷酸受体调节剂 (S1PRM) 反应不足或不耐受的受试者。
在 UC-1 中,基线时 mMS 中位数为 7;37% 的患者病情严重(mMS >7);69% 的患者 ES 为 3。在 UC-1 中,52% (499/966) 的受试者使用一种或多种生物制剂、JAKi 或 S1PRM 治疗失败(反应不足或不耐受)。在这 499 名受试者中,484 名 (97%) 的生物制剂治疗失败,90 名 (18%) 的 JAK 抑制剂治疗失败。入组受试者可以使用稳定剂量的口服皮质类固醇(最高 20 mg/天泼尼松或等效剂量)、免疫调节剂和氨基水杨酸盐。在基线时,36% 的受试者正在接受皮质类固醇治疗,16% 的受试者正在接受免疫调节剂(包括硫唑嘌呤、6-巯基嘌呤、甲氨蝶呤),73% 的受试者正在接受 UC-1 中的氨基水杨酸盐治疗。
在 UC-1 中,主要终点是第 12 周使用 mMS 定义的临床缓解(见表 13)。关键次要终点包括临床反应、内镜改善和组织学内镜粘膜改善(见表13)。
| 端点 | 安慰剂 | SKYRIZI 1,200 毫克静脉输液 | 治疗差异 (95% CI) b |
| 临床缓解c | |||
| 总人口 | 人数=320 8% |
人数=646 24% |
16%小时 (12%, 20%) |
| 先前的生物制剂、JAKi 或 S1PRM 失败d | 样本量:168 6% |
人数=331 14% |
|
| 没有先前的生物制剂、JAKi 或 S1PRM 失败 | 人数=152 9% |
人数=315 33% |
|
| 临床反应 | |||
| 总人口 | 人数=320 36% |
人数=646 65% |
29%小时 (23%, 35%) |
| 先前的生物制剂、JAKi 或 S1PRM 失败d | 人数=168 32% |
人数=331 56% |
|
| 没有先前的生物制剂、JAKi 或 S1PRM 失败 | 人数=152 41% |
人数=315 75% |
|
| 内窥镜改进 | |||
| 总人口 | 人数=320 12% |
人数=646 36% |
25%小时 (20%,30%) |
| 先前的生物制剂、JAKi 或 S1PRM 失败d | 人数=168 10% |
人数=331 26% |
|
| 没有先前的生物制剂、JAKi 或 S1PRM 失败 | 人数=152 14% |
人数=315 47% |
|
| 组织学内镜粘膜改善 (HEMI) g | |||
| 总人口 | 样本量:320 7% |
人数=646 24% |
17%小时 (13%, 21%) |
| 先前的生物制剂、JAKi 或 S1PRM 失败d | 人数=168 7% |
人数=331 16% |
|
| 没有先前的生物制剂、JAKi 或 S1PRM 失败 | 样本量:152 8% |
人数=315 33% |
|
| a 在第 0 周、第 4 周和第 8 周以静脉输注方式给予 SKYRIZI 1,200 mg b 基于Cochran-Mantel-Haenszel 方法调整分层因素后的调整治疗差异(95% CI) c每 mMS:SFS ≤ 1 且不大于基线,RBS = 0,且 ES ≤ 1 无易碎性 d先前失败包括对以下一种或多种治疗反应不足或不耐受:生物疗法、Janus 激酶抑制剂 (JAKi) 和/或鞘氨醇-1-磷酸受体调节剂 (S1PRM) e每 mMS:较基线下降 ≥ 2 分且 ≥ 30%,且 RBS 较基线下降 ≥ 1 或绝对 RBS ≤ 1 f ES ≤ 1,无易碎性证据 g ES ≤ 1,无易碎性证据且 Geboes 评分 ≤ 3.1(表明中性粒细胞浸润在 <5% 的隐窝中,没有隐窝破坏,也没有糜烂、溃疡或肉芽组织) h p < 0.001 |
|||
UC-1 并非旨在评估第 12 周组织学内镜粘膜改善与病情进展和长期结果之间的关系。
直肠出血和排便频率子评分
与安慰剂组相比,早在 4 周时就观察到使用 SKYRIZI 治疗的受试者的直肠出血和排便频率子评分有所下降。
内窥镜评估
内镜缓解定义为 ES 为 0。在第 12 周,与安慰剂组相比,使用 SKYRIZI 治疗的受试者中有更大比例达到内镜缓解(11% 对 3%)。
排便紧迫感
与安慰剂相比,接受 SKYRIZI 1,200 毫克诱导方案治疗的受试者在第 12 周时没有出现排便紧迫感的比例更高(44% 对 27%)。
疲劳
在 UC-1 中,与接受安慰剂治疗的受试者相比,接受 SKYRIZI 治疗的受试者在第 12 周时疲劳症状有显著改善,以 FACIT-F 评分相对于基线的变化来评估。SKYRIZI 在诱导治疗 12 周后改善疲劳的效果尚未确定。
其他 UC 症状
第 12 周时,接受 SKYRIZI 治疗的受试者中没有夜间排便的受试者比例高于接受安慰剂治疗的受试者(67% vs 43%)。
UC-2维护研究
维持研究 (UC-2; NCT03398135) 评估了 547 名受试者,这些受试者在 UC-1 或 UC-3 研究中接受了三种 SKYRIZI 诱导方案之一(包括 1,200 毫克方案)治疗 12 周,并在 12 周后根据 mMS 显示出临床反应。受试者在第 12 周随机接受皮下 (SC) SKYRIZI 180 毫克或 SKYRIZI 360 毫克或安慰剂维持方案,此后每 8 周接受一次,最多再接受 52 周。
在 UC-2 中,75% (411/547) 的受试者使用一种或多种生物制剂、JAKi 或 S1PRM 治疗失败(反应不足或不耐受)。在这 411 名受试者中,407 名 (99%) 的生物制剂治疗失败,78 名 (19%) 的 JAK 抑制剂治疗失败。
UC-2 的主要终点是第 52 周使用 mMS 的临床缓解情况(见表14)。关键次要终点包括无皮质类固醇临床缓解、内镜检查改善和组织学内镜黏膜改善(见表14)。
| 端点 | 安慰剂 | SKYRIZI 180 毫克 SC 注射剂b |
SKYRIZI 360 毫克 SC 注射剂c |
| 临床缓解d | |||
| 总人口 | 人数=182 26% |
人数=179 45% |
人数=186 41% |
| 与安慰剂相比的治疗差异(95% CI) | 20% [ 11%, 29%] |
16% [ 7%, 25%] |
|
| 先前的生物制剂、JAKi 或 S1PRM 失败f | 人数=138 24% |
人数=134 41% |
人数=139 32% |
| 没有先前的生物制剂、JAKi 或 S1PRM 失败 | 人数=44 32% |
人数=45 58% |
人数=47 67% |
| 不服用皮质类固醇的临床缓解 | |||
| 总人口 | 人数=182 26% |
人数=179 45% |
人数=186 40% |
| 与安慰剂相比的治疗差异(95% CI) | 20% [ 11%, 29%] |
16% [ 7%, 25%] |
|
| 先前的生物制剂、JAKi 或 S1PRM 失败f | 人数=138 24% |
人数=134 40% |
人数=139 32% |
| 没有先前的生物制剂、JAKi 或 S1PRM 失败 | 人数=44 32% |
人数=45 58% |
人数=47 64% |
| 内镜改善h | |||
| 总人口 | 样本量:182 31% |
人数=179 51% |
人数=186 48% |
| 与安慰剂相比的治疗差异(95% CI) | 20% [ 11%, 30%] |
18% [ 8%, 27%] |
|
| 先前的生物制剂、JAKi 或 S1PRM 失败f | 人数=138 30% |
人数=134 48% |
人数=139 39% |
| 没有先前的生物制剂、JAKi 或 S1PRM 失败 | 人数=44 34% |
人数=45 60% |
人数=47 76% |
| 组织学内镜黏膜改善i | |||
| 总人口 | 样本量:182 24% |
样本量:179 43% |
人数=186 42% |
| 与安慰剂相比的治疗差异(95% CI) | 20% [ 11%, 29%] |
20% [ 11%, 29%] |
|
| 先前的生物制剂、JAKi 或 S1PRM 失败f | 人数=138 22% |
人数=134 39% |
人数=139 33% |
| 没有先前的生物制剂、JAKi 或 S1PRM 失败 | 人数=44 30% |
人数=45 55% |
人数=47 69% |
| a安慰剂组由对 12 周 SKYRIZI 诱导治疗有反应的受试者组成,并在维持治疗开始时随机接受安慰剂。 b第 12 周时服用 180 mg SKYRIZI,之后每 8 周服用一次,最多服用 52 周 c第 12 周时服用 360 mg SKYRIZI,之后每 8 周服用一次,最多服用 52 周 d每 mMS:SFS ≤ 1 且不大于基线,RBS = 0,且 ES ≤ 1 无易碎性 e基于 Cochran-Mantel-Haenszel 方法调整后的治疗差异 (95% CI),并根据分层因素进行了调整 f先前的失败包括对以下一种或多种治疗反应不足或不耐受:生物疗法、Janus 激酶抑制剂 (JAKi) 和/或鞘氨醇-1-磷酸受体调节剂 (S1PRM) g第 52 周时每 mMS 的临床缓解率,并且停用皮质类固醇≥90 天 h ES ≤ 1,无易碎性证据 i ES ≤ 1,无易碎性证据,并且 Geboes 评分≤ 3.1(表示中性粒细胞浸润在<5%的隐窝中,无隐窝破坏,无糜烂、溃疡或肉芽组织) j p < 0.001 |
|||
内窥镜评估
内镜缓解定义为 ES 为 0。在 UC-2 中,与安慰剂相比,接受 SKYRIZI 180 mg 和 SKYRIZI 360 mg 治疗的受试者中有更大比例在第 52 周达到内镜缓解(分别为 23% 和 24% vs 15%)。
16. Skyrizi 注射液如何供应
如何供应
SKYRIZI(risankizumab-rzaa)注射剂具有以下强度:
| 力量 | 包装尺寸 | 国家数据中心 |
| 皮下注射 | ||
| 150 mg/mL 单剂量注射笔 | 纸箱 1 | 0074-2100-01 |
| 90 mg/mL 单剂量预充式注射器 | 纸箱 2 件 | 0074-7040-02 |
| 纸箱 4 件 | 0074-7042-04 | |
| 150 mg/mL 单剂量预充式注射器 | 纸箱 1 | 0074-1050-01 |
| 180 mg/1.2 mL(150 mg/mL)单剂量预充药筒,带随身注射器 | 成套工具 | 0074-1065-01 |
| 360 mg/2.4 mL(150 mg/mL)单剂量预充药筒,带随身注射器 | 成套工具 | 0074-1070-01 |
| 静脉输液 | ||
| 600 mg/10 mL(60 mg/mL)单剂量小瓶 | 纸箱 1 | 0074-5015-01 |
皮下注射
SKYRIZI 150 mg/mL 预充式注射器或预充式注射笔含有无菌、无防腐剂、无色至黄色、透明至微乳白色的溶液。每个预充式注射器或预充式注射笔均由 1 mL 玻璃注射器和固定的 27 号 ½ 英寸针头(带针头保护器)组成。
SKYRIZI 90 mg/mL 预充式注射器是一种无菌、无防腐剂、无色至微黄色和透明至微乳白色的溶液。每个预充式注射器由一个 1 mL 玻璃注射器和一个固定的 29 号 ½ 英寸针头(带针头保护器)组成。
SKYRIZI 180 mg/1.2 mL(150 mg/mL)环烯烃聚合物预充式药筒带有隔膜和盖子,含有无菌、无防腐剂、无色至黄色、透明至微乳白色的溶液,可与随附的体内注射器给药装置一起使用。
SKYRIZI 360 mg/2.4 mL(150 mg/mL)环烯烃聚合物预充式药筒带有隔膜和盖子,含有无菌、无防腐剂、无色至黄色、透明至微乳白色的溶液,可与随附的体内注射器给药装置一起使用。
静脉输液
SKYRIZI 600 mg/10 mL(60 mg/mL)小瓶含有无菌、无防腐剂、无色至微黄色、透明至微乳白色的溶液。每个玻璃小瓶都用塞子和蓝色翻盖封闭。
储存和处理
- 存放在 36°F 至 46°F(2°C 至 8°C)的冰箱中。
- 不要冻结。
- 请勿摇晃。
- 保存在原纸箱中以避光。
- 不是采用天然橡胶乳胶制成的。
17. 患者咨询信息
建议患者和/或护理人员阅读 FDA 批准的患者标签(用药指南和使用说明)。
超敏反应
建议患者如果出现任何严重超敏反应症状,应停止使用 SKYRIZI 并立即就医[见警告和注意事项 ( 5.1 )]。
感染
告知患者 SKYRIZI 可能会降低其免疫系统抵抗感染的能力。指导患者向医疗保健提供者通报任何感染史的重要性,并在出现任何感染症状时联系其医疗保健提供者[见警告和注意事项 ( 5.2 )]。
炎症性肠病治疗中的肝毒性
告知患者 SKYRIZI 可能导致肝损伤,尤其是在治疗的最初 12 周内。指导患者如果出现提示肝功能障碍的症状,应立即就医。(例如,不明原因的皮疹、恶心、呕吐、腹痛、疲劳、厌食或黄疸和/或深色尿液)[见警告和注意事项 ( 5.4 )] 。
疫苗接种
告知患者,在 SKYRIZI 治疗期间以及 SKYRIZI 治疗之前或之后不建议接种活疫苗。与免疫系统相互作用的药物可能会增加接种活疫苗后感染的风险。指导患者在可能接种疫苗之前告知医疗保健从业者他们正在服用 SKYRIZI [见警告和注意事项( 5.5 ) ]。
管理指令
指导患者或护理人员在合格医疗专业人员的监督和指导下进行首次自我注射剂量,以培训 SKYRIZI 的准备和管理,包括选择给药的解剖部位,以及正确的皮下注射技术[见使用说明]。
如果使用 SKYRIZI 90 mg/mL,指导患者或护理人员使用两支 90 mg 单剂量注射器注射以达到治疗克罗恩病的 SKYRIZI 的全部 180 mg 维持剂量,或使用四支 90 mg 单剂量注射器注射以达到治疗克罗恩病的 SKYRIZI 的全部 360 mg 维持剂量[见使用说明]。
指导患者或护理人员如何处置笔或注射器[见使用说明]。
怀孕
告知患者,有一个妊娠登记处可以监测妊娠期间接触 SKYRIZI 的女性的妊娠结果[见特定人群中的使用(8.1)]。
制造商:
AbbVie Inc.
美国伊利诺伊州北芝加哥 60064
美国许可证号 1889
SKYRIZI ®是 AbbVie Biotechnology Ltd. 的注册商标。
© 2019-2024 AbbVie Inc.
20086179 R2 6/2024
用药指南
| 用药指南SKYRIZI ® (sky-RIZZ-ee) (risankizumab-rzaa)注射剂,供皮下或静脉使用 |
|||||||
| 关于 SKYRIZI,我应该知道的最重要的信息是什么? SKYRIZI 可能导致严重的副作用,包括: 严重的过敏反应。如果您出现以下任何严重过敏反应症状,请停止使用 SKYRIZI 并立即寻求紧急医疗帮助: |
|||||||
| ● 昏厥、头晕、头昏眼花(低血压) | ● 胸闷 |
||||||
| ● 面部、眼睑、嘴唇、口腔、舌头或喉咙肿胀 | ● 皮疹、荨麻疹 | ||||||
| ● 呼吸困难或喉咙紧绷 | ● 瘙痒 | ||||||
| 感染。SKYRIZI可能会降低您的免疫系统抵抗感染的能力,并可能增加您感染的风险。您的医疗保健提供者应在开始使用 SKYRIZI 治疗之前检查您是否感染和结核病 (TB),如果您有结核病史或患有活动性结核病,则可能在您开始使用 SKYRIZI 治疗之前为您治疗结核病。您的医疗保健提供者应在使用 SKYRIZI 治疗期间和治疗后密切观察您是否出现结核病的体征和症状。如果您感染或出现感染症状,请立即告知您的医疗保健提供者,包括: | |||||||
| ● 发烧、出汗或发冷 | ● 肌肉酸痛 | ● 减肥 | |||||
| ● 咳嗽 | ● 身体出现与牛皮癣不同的发热、发红或疼痛的皮肤或疮疡 | ● 腹泻或胃痛 | |||||
| ● 呼吸困难 | ● 排尿时有灼烧感或排尿次数比平时多 | ||||||
| ● 粘液 (痰)中带血 |
|||||||
| 有关副作用的更多信息,请参阅“SKYRIZI 可能出现哪些副作用?” 。 | |||||||
SKYRIZI 是什么?
|
|||||||
| 哪些人不应使用 SKYRIZI? 如果您对 risankizumab-rzaa 或 SKYRIZI 中的任何成分过敏,请勿使用 SKYRIZI。请参阅本用药指南末尾的 SKYRIZI 完整成分列表。 |
|||||||
在使用 SKYRIZI 之前,请告知您的医疗保健提供者您的所有医疗状况,包括:
告知您的医疗保健提供者您服用的所有药物,包括处方药和非处方药、维生素和草药补充剂。 |
|||||||
我应该如何使用 SKYRIZI?
患有斑块状银屑病或银屑病关节炎的成人患者将使用预充式注射笔或预充式注射器接受 SKYRIZI 皮下注射(皮下注射)。 |
|||||||
SKYRIZI 可能产生哪些副作用?
|
|||||||
|
|
|
|
||||
| 对于接受克罗恩病治疗的患者来说, S KYRIZI最常见的副作用包括溃疡性结肠炎: | |||||||
|
|
|
|||||
| 对于接受斑块状银屑病和银屑病关节炎治疗的患者,SKYRIZI 最常见的副作用包括: | |||||||
|
|
||||||
| 这些并不是 SKYRIZI 的所有可能副作用。 请致电您的医生获取有关副作用的医疗建议。您可以拨打 1-800-FDA-1088 向 FDA 报告副作用。 |
|||||||
我应该如何储存 SKYRIZI?
请将 SKYRIZI 和所有药物放在儿童接触不到的地方。 |
|||||||
| 有关安全有效使用 SKYRIZI 的一般信息。 有时医生会开具药物指南中未列出的其他用途的处方药。请勿将 SKYRIZI 用于未规定的病症。请勿将 SKYRIZI 给其他人服用,即使他们有与您相同的症状。这可能会伤害他们。您可以向您的药剂师或医疗保健提供者询问有关 SKYRIZI 的针对健康专业人士编写的信息。 |
|||||||
| SKYRIZI中含有哪些成分? 活性成分: risankizumab-rzaa。SKYRIZI 90 mg/mL非活性成分:聚山梨醇酯 20、琥珀酸钠、山梨醇、琥珀酸和注射用水(USP)。SKYRIZI 150 mg/mL、180 mg/1.2 mL、360 mg/2.4 mL 和 600 mg/ 10 mL非活性成分:冰醋酸、聚山梨醇酯 20、醋酸钠、海藻糖和注射用水(USP)。制造商:AbbVie Inc.,美国伊利诺伊州北芝加哥 60064美国许可证号 1889 SKYRIZI ®是 AbbVie Biotechnology Ltd. 的注册商标。© 2019-2024 AbbVie Inc.如需了解更多信息,请致电 1-866-SKYRIZI (1-866-759-7494) 或访问 www.SKYRIZI.com。 |
|||||||
| 本用药指南已获美国食品药品管理局 20086179 R2批准 |
修订日期:6/2024 | ||||||
使用说明SKYRIZI ® (sky-RIZZ-ee) Pen (risankizumab-rzaa)注射剂,供皮下使用
首次使用前请阅读
有关产品信息,请参阅用药指南。
在使用 SKYRIZI Pen (risankizumab-rzaa) 注射剂之前,请阅读本使用说明。
在使用 SKYRIZI 之前,您应该接受医疗保健提供者关于如何注射 SKYRIZI 的培训。
SKYRIZI 单剂量注射笔

重要信息
- 将 SKYRIZI 存放在36°F 至 46°F (2°C 至 8°C) 的冰箱中。
- 将 SKYRIZI 放在原装纸盒中避光保存,直到您准备使用为止。
- 注射前,将 SKYRIZI 纸盒从冰箱中取出。将纸盒放置于室温下并避免阳光直射30 至 90 分钟。
- 检查窗中的液体应看起来透明至黄色,并可能含有微小的白色或透明颗粒。
- 如果液体变色、浑浊 或含有薄片或大颗粒,请勿使用 SKYRIZI 。
- 如果已超过有效期 (EXP),请勿使用 SKYRIZI 。
- 如果液体已经冻结,请勿使用 SKYRIZI ,即使已经解冻。
- 不要摇晃 SKYRIZI。
- 如果 SKYRIZI Pen 已掉落或损坏,请勿使用。
- 如果纸盒穿孔破损,请勿使用 SKYRIZI 。请将产品退回药房。
- 注射前请勿取下深灰色盖子。
- SKYRIZI 不是采用天然橡胶乳胶制成的。
准备 SKYRIZI 注射剂 |
将SKYRIZI 纸盒从冰箱中取出。注射前,将纸盒放置在室温下,避免阳光直射30 至 90 分钟。
|
|
检查有效期(EXP)。如果已过有效期,请勿使用笔。
洗净并擦干双手。 |
|
选择注射部位:
用酒精棉签以圆周运动的方式擦拭注射部位并让其干燥。 |
|
握住笔,使深灰色笔帽朝上。
通过检查窗检查液体。
|
注射 SKYRIZI |
用手指握住注射笔的灰色手柄。转动 |
|
握住注射笔,以便您能看到绿色激活按钮和检查窗口。将注射笔推入凸起的注射部位
按下绿色激活按钮并按住笔15秒。
|
|
继续将注射笔压在注射部位。
这最多需要 15秒。 |
SKYRIZI 注射后 |
注射完成后,慢慢将注射笔从皮肤中拉出。
|
|
使用后立即将用过的笔扔进FDA批准的锐器处理容器中。 ●除非社区准则允许,否则请勿将用过的笔丢弃在家庭垃圾中。 ●请勿回收锐器处理容器。深灰色笔帽、酒精棉签、棉球或纱布垫以及包装可放入家庭垃圾中。有关更多信息,请参阅“用过的 SKYRIZI 预充式笔处理” 。 |
重要信息
- 将 SKYRIZI 存放在36°F 至 46°F (2°C 至 8°C) 的冰箱中。
- 将 SKYRIZI 放在原装纸盒中避光保存,直到您准备使用为止。
- 注射前,将 SKYRIZI 纸盒从冰箱中取出。将纸盒放置在室温下,避免阳光直射30 至 90 分钟。
- 检查窗中的液体应看起来透明至黄色,并可能含有微小的白色或透明颗粒。
- 如果液体变色、浑浊或含有薄片或大颗粒,请勿使用 SKYRIZI 。
- 如果已超过有效期 (EXP),请勿使用 SKYRIZI 。
- 如果液体已经冻结,请勿使用 SKYRIZI ,即使已经解冻。
- 不要摇晃 SKYRIZI。
- 如果 SKYRIZI Pen 已掉落或损坏,请勿使用。
- 如果纸盒穿孔破损,请勿使用 SKYRIZI 。请将产品退回药房。
- 注射前请勿取下深灰色盖子。
- SKYRIZI 不是采用天然橡胶乳胶制成的。
请将SKYRIZI笔和锐器处理容器放在儿童接触不到的地方。
如果您需要帮助或不知道如何继续,请致电您的医疗保健提供者或(866) SKYRIZI 或 (866) 759-7494 。
关于使用 SKYRIZI 笔的问题
问: 如果我需要有关如何注射 SKYRIZI 的帮助怎么办?
答.如果您需要帮助, 请致电您的医疗保健提供者或 (866) SKYRIZI 或 (866) 759-7494 。
问: 我取下了深灰色盖子并按下了绿色激活按钮。为什么我的注射没有开始?
答: 除非将白色针套用力按在注射部位,否则绿色激活按钮不会开始注射。
问: 我如何知道注射何时完成?
答: 如果注射笔发出第二次“咔哒”声或黄色指示器充满检查窗口,则表示注射完成。这最多需要15秒。
问: 如果注射部位有超过几滴液体,我该怎么办?
答. 致电 (866) SKYRIZI 或 (866) 759-7494 寻求帮助。
问: 注射后,我该如何处理用过的注射笔?
A. 使用后立即将用过的笔丢弃到锐器处理容器中。请勿将用过的笔丢弃到家庭垃圾中。
您可以访问www. SKYRIZI .com或致电(866) SKYRIZI或 (866) 759-7494注册以获得用于 SKYRIZI Pen 处理的锐器容器,无需支付额外费用。
请致电 (866) SKYRIZI或 (866) 759-7494或访问 www. SKYRIZI .com 获取注射帮助。
 |
为了帮助记住何时注射,请在日历上标记您注射 SKYRIZI 的日期。 |
请将SKYRIZI笔和锐器处理容器放在儿童接触不到的地方。
如果您需要帮助或对使用 SKYRIZI 有任何疑问,请致电您的医疗保健提供者或 (866) SKYRIZI 或 (866) 759-7494。
已使用 SKYRIZI 预充注射笔的处置
如果您没有经 FDA 批准的锐器处理容器,您可以使用符合以下要求的家用容器:
- 由耐用塑料制成,
- 可以用紧密贴合、防刺穿的盖子盖上,不会有尖锐物体掉出来,
- 使用时直立且稳定,
- 防漏,
- 正确标记以警告容器内有危险废物。
当您的锐器处理容器快要装满时,您需要遵循社区指南,以正确方式处理锐器处理容器。州或地方法律可能规定了如何丢弃用过的钢笔。
有关安全锐器处理的更多信息,以及您所在州的锐器处理的具体信息,请访问 FDA 网站:www.fda.gov/safesharpsdisposal。
请勿回收使用过的锐器处理容器。
制造商:AbbVie Inc.,美国伊利诺伊州北芝加哥 60064
美国许可证号 1889
SKYRIZI ®是 AbbVie Biotechnology Ltd. 的注册商标。
© 2019-2024 AbbVie Inc.
20086179
本使用说明已获得美国食品药品管理局的批准。
修订日期:6/2024
使用说明SKYRIZI ® (sky-RIZZ-ee) (risankizumab-rzaa)注射剂,供皮下使用150 mg/mL 预充式注射器
首次使用前请阅读
有关产品信息,请参阅用药指南。
SKYRIZI 单剂量预充注射器

重要信息
- 将 SKYRIZI 放在原装纸盒中,避免光照,直至使用。
- 该液体看起来应为透明至黄色,并且可能含有微小的白色或透明颗粒。
- 如果液体变色、浑浊或含有薄片或大颗粒,请勿使用 SKYRIZI 。
- 如果纸盒和预充注射器上显示的有效期 (EXP:)已过,请勿使用 SKYRIZI 。
- 如果液体已经冻结(即使解冻),请勿使用 SKYRIZI。
- 不要摇晃 SKYRIZI。
- 如果预充注射器掉落或损坏,请勿使用 SKYRIZI 。
- 如果纸盒穿孔破损,请勿使用 SKYRIZI 。请将产品退回药房。
- 在注射之前请勿取下针头盖。
请将 SKYRIZI 和所有药物放在儿童接触不到的地方。
使用 SKYRIZI预充式注射器前请阅读完整的使用说明
注射前
- 注射前接受有关如何注射 SKYRIZI 的培训。如需帮助,请致电您的医疗保健提供者或(866) SKYRIZI 或 (866) 759-7494 。
- 提前在日历上做个标记,以记住何时服用 SKYRIZI。
- 将纸箱放置于室温下,避免阳光直射,放置15 至 30 分钟以使其变暖。
- 让 SKYRIZI 达到室温时,请勿将注射器从纸箱中取出。
- 请勿以任何其他方式加热 SKYRIZI(例如,请勿在微波炉或热水中加热)。
- 让 SKYRIZI 达到室温时,请勿将注射器从纸箱中取出。
重要信息
- 该液体看起来应为透明至黄色,并且可能含有微小的白色或透明颗粒。
- 如果液体变色、浑浊或含有薄片或大颗粒,请勿使用 SKYRIZI 。
- 如果纸盒和预充注射器上显示的有效期 (EXP:)已过,请勿使用 SKYRIZI 。
- 如果注射器掉落或损坏,请勿使用 SKYRIZI 。
- 如果纸盒穿孔破损,请勿使用 SKYRIZI 。请将产品退回药房。
存储信息
- 将 SKYRIZI 存放在 36°F 至 46°F (2°C 至 8°C) 的冰箱中。
- 不要摇晃 SKYRIZI。
- 将 SKYRIZI 放在原装纸盒中,避免光照,直至使用。
- SKYRIZI 不是采用天然橡胶乳胶制成的。
- 如果液体已冻结(即使解冻),请勿使用。
请将 SKYRIZI 和所有药物放在儿童接触不到的地方。
如果您需要帮助或不知道如何继续,请致电您的医疗保健提供者或(866) SKYRIZI 或 (866) 759-7494。
|
收集注射所需的用品。
将以下物品放置在干净、平坦的表面上:
洗净并擦干双手。 |
|
|
握住手指,从纸板套中取出预充式注射器。 |
|
|
从 3 个可注射区域中选择:
注射前,用酒精棉签以圆周运动的方式擦拭注射部位。
|
|
|
握住预充式注射器,针头朝下,如图所示。
|
|
|
取下针盖。
|
|
|
一只手用拇指和食指握住预充式注射器的主体。另一只手 |
|
|
慢慢将柱塞杆推入,直到所有液体都注入,预充式注射器已空。
|
|
|
使用后,请立即将用过的预充式注射器放入FDA 批准的锐器处理容器中。
有关更多信息,请参阅“使用过的 SKYRIZI 预充式注射器处理”部分。 |
关于使用 SKYRIZI 的问题
| 问:如果我需要有关如何注射 SKYRIZI 的帮助怎么办? |
| 答.如果您需要帮助,请致电您的医疗保健提供者或(866) SKYRIZI 或 (866) 759-7494 。 |
| 问:注射后,我该如何处理用过的预充式注射器? |
| 答:将使用过的预充式注射器扔进锐器处理容器,而不是扔进家庭垃圾中。您可以访问www.SKYRIZI .com或致电(866) SKYRIZI 或 (866) 759-7494 ,注册免费获得用于 SKYRIZI 注射器处理的锐器容器。 |
问:我如何知道注射何时完成? |
| A. 当预充式注射器为空、柱塞杆完全推入、注射器针头保护装置启动时,注射完成。 |
使用过的 SKYRIZI 预充式注射器处理
如果您没有经 FDA 批准的锐器处理容器,您可以使用符合以下要求的家用容器:
- 由耐用塑料制成,
- 可以用紧密贴合、防刺穿的盖子盖上,不会有尖锐物体掉出来,
- 使用时直立且稳定,
- 防漏,
- 正确标记以警告容器内有危险废物。
当您的锐器处理容器快要装满时,您需要遵循社区指南,以正确方式处理锐器处理容器。州或地方法律可能规定了如何丢弃用过的针头和注射器。
有关安全锐器处理的更多信息,以及您所在州的锐器处理的具体信息,请访问 FDA 网站:www.fda.gov/safesharpsdisposal。
请勿回收使用过的锐器处理容器。
制造商:AbbVie Inc.,美国伊利诺伊州北芝加哥 60064
美国许可证号 1889
SKYRIZI ®是 AbbVie Biotechnology Ltd. 的注册商标。
© 2019-2024 AbbVie Inc.
20086082
本使用说明已获得美国食品药品管理局的批准。
修订日期:6/2024
使用说明SKYRIZI ® (sky-RIZZ-ee) (risankizumab-rzaa)注射液,皮下注射
2 x 90 mg/mL 单剂量预充式注射器,总剂量为 180 mg/2 mL
首次使用前请阅读
有关产品信息,请参阅用药指南。
SKYRIZI 单剂量预充注射器

请将 SKYRIZI 和所有药物放在儿童接触不到的地方。
重要信息:
- 将 SKYRIZI 放在原装纸盒中,避免光照,直至使用。
- 液体看起来应透明至微黄色,并可能含有微小的白色或透明颗粒。
- 如果液体变色、浑浊或含有薄片或大颗粒,请勿使用 SKYRIZI 。请将产品退回药房。
- 如果纸盒和预充式注射器上显示的有效期 (EXP:)已过,请勿使用 SKYRIZI 。将产品退回药房。
- 如果液体已经冻结(即使解冻),请勿使用 SKYRIZI。
- 不要摇晃注射器。
- 如果预充式注射器掉落或损坏,请勿使用 SKYRIZI 。请将产品退回药房。
- 如果纸盒穿孔破损,请勿使用 SKYRIZI 。请将产品退回药房。
- 在注射之前请勿取下针头盖。
- SKYRIZI 不是采用天然橡胶乳胶制成的。
使用 SKYRIZI 预充式注射器前请阅读完整的使用说明
注射前:
- 注射前接受有关如何注射SKYRIZI 的培训。如需帮助,请致电您的医疗保健提供者或(866) SKYRIZI 或 (866) 759-7494 。
- 提前在日历上做个标记,以记住何时服用 SKYRIZI。
- 将纸箱放置于室温下,避免阳光直射,放置15 至 30 分钟以使其变暖。
- 让 SKYRIZI 达到室温时,请勿从纸箱中取出预充注射器。
- 请勿以任何其他方式加热 SKYRIZI(例如,请勿在微波炉或热水中加热)。
- 让 SKYRIZI 达到室温时,请勿从纸箱中取出预充注射器。
重要 信息:
- 液体看起来应透明至微黄色,并可能含有微小的白色或透明颗粒。
- 如果液体变色、浑浊或含有薄片或大 颗粒,请勿使用 SKYRIZI 。请将产品退回 药房。
- 如果纸盒和预充式注射器上显示的有效期 (EXP:) 已过,请勿使用 SKYRIZI。将产品退回药房。
- 如果预充式注射器掉落或损坏,请勿使用SKYRIZI 。请将产品退回药房。
- 如果纸盒穿孔破损,请勿使用SKYRIZI 。请将产品退回药房。
存储信息:
- 将 SKYRIZI 存放在36°F 至 46°F (2°C 至 8°C)的冰箱中。
- 不要摇晃 SKYRIZI。
- 将 SKYRIZI 放在原装纸盒中,避免光照,直至使用。
- SKYRIZI 不是采用天然橡胶乳胶制成的。
- 如果液体已冻结(即使已解冻),请勿使用。
请将 SKYRIZI 和所有药物放在儿童接触不到的地方。
如果您需要帮助或不知道如何继续,请致电您的医疗保健提供者或(866) SKYRIZI或(866) 759-7494。
|
洗净并擦干双手。 |
|
从 3 个可注射区域中选择:
|
|
握住预充式注射器,针头朝下,如图所示。
|
|
取下针盖。
|
|
一只手用拇指和食指握住预充式注射器的主体。另一只手 |
|
慢慢将柱塞杆推到底,直到所有液体都注入,注射器空了。保持注射器的角度不变,将针头从皮肤中拔出。
除非所有液体都已注入,否则针头保护装置不会自动启动。
|
|
使用第二支预充式注射器重复步骤 2 至 6,以获得完整剂量。
|
|
使用后,请立即将用过的预充式注射器放入FDA 批准的锐器处理容器中。
如需更多信息,或如果您没有 FDA 批准的锐器容器,请参阅这些说明另一侧的“使用过的 SKYRIZI 预充式注射器处理”部分。 |
关于使用 SKYRIZI 注射器的问题
问: 如果我没有接受过医疗专业人员的面对面培训怎么办?
答:如果您需要帮助,请致电您的医疗保健提供者或(866) SKYRIZI或(866) 759-7494 。在注射前接受有关如何注射SKYRIZI 的培训。
问:注射后,我应该如何处理两个用过的预充式注射器?
A. 将两个用过的预充式注射器扔进锐器处理容器中。不要扔进家庭垃圾中。有关更多信息,请参阅“用过的 SKYRIZI 预充式注射器处理”部分。
您可以访问 www.SKYRIZI.com 或致电 (866) 759-7494,注册获得用于 SKYRIZI 预充式注射器处置的锐器容器,无需支付额外费用
问:我如何知道注射何时完成?
A. 当预充式注射器为空、柱塞杆完全推入、注射器针头保护装置启动时,注射完成。
使用过的 SKYRIZI 预充式注射器处理
将两个用过的预充式注射器扔进锐器处理容器中。不要扔进家庭垃圾中。
如果您没有经 FDA 批准的锐器处理容器,您可以使用以下家用容器:
- 由重型塑料制成,
- 可以用紧密贴合、防刺穿的盖子盖上,不会有尖锐物体掉出来,
- 使用过程中保持直立和稳定,
- 防漏,并且
- 已正确贴上标签,警告容器内有危险废物。
当您的锐器处理容器快要装满时,您需要遵循社区指南,以正确方式处理锐器处理容器。州或地方法律可能规定了如何丢弃用过的针头和注射器。
有关安全锐器处理的更多信息,以及您所在州的锐器处理的具体信息,请访问 FDA 网站:www.fda.gov/safesharpsdisposal。
请勿回收使用过的锐器处理容器。
制造商:AbbVie Inc.,美国伊利诺伊州北芝加哥 60064
美国许可证号 1889
SKYRIZI ®是 AbbVie Biotechnology Ltd. 的商标。
© 2019-2024 AbbVie Inc.
20078139
本使用说明已获得美国食品药品管理局的批准。
修订日期:2024 年 3 月
使用说明SKYRIZI ® (sky-RIZZ-ee) (risankizumab-rzaa)注射剂,供皮下使用4 x 90 mg/mL 单剂量预充式注射器,总剂量为 360 mg/4 mL
首次使用前请阅读
有关产品信息,请参阅用药指南。
SKYRIZI 单剂量预充注射器

请将 SKYRIZI 和所有药物放在儿童接触不到的地方。
重要信息:
- 将 SKYRIZI 放在原装纸盒中,避免光照,直至使用。
- 液体看起来应透明至微黄色,并可能含有微小的白色或透明颗粒。
- 如果液体变色、浑浊或含有薄片或大颗粒,请勿使用 SKYRIZI 。请将产品退回药房。
- 如果纸盒和预充式注射器上显示的有效期 (EXP:)已过,请勿使用 SKYRIZI 。将产品退回药房。
- 如果液体已经冻结(即使解冻),请勿使用 SKYRIZI。
- 不要摇晃注射器。
- 如果预充式注射器掉落或损坏,请勿使用 SKYRIZI 。请将产品退回药房。
- 如果纸盒穿孔破损,请勿使用 SKYRIZI 。请将产品退回药房。
- 在注射之前请勿取下针头盖。
- SKYRIZI 不是采用天然橡胶乳胶制成的。
使用 SKYRIZI 预充式注射器前请阅读完整的使用说明
注射前:
- 注射前接受有关如何注射SKYRIZI 的培训。如需帮助,请致电您的医疗保健提供者或(866) SKYRIZI 或 (866) 759-7494 。
- 提前在日历上做个标记,以记住何时服用 SKYRIZI。
- 将纸箱放置于室温下,避免阳光直射,放置15 至 30 分钟以使其变暖。
- 让 SKYRIZI 达到室温时,请勿从纸箱中取出预充注射器。
- 请勿以任何其他方式加热 SKYRIZI(例如,请勿在微波炉或热水中加热)。
- 让 SKYRIZI 达到室温时,请勿从纸箱中取出预充注射器。
重要 信息:
- 液体看起来应透明至微黄色,并可能含有微小的白色或透明颗粒。
- 如果液体变色、浑浊或含有薄片或大 颗粒,请勿使用 SKYRIZI 。请将产品退回 药房。
- 如果纸盒和预充式注射器上显示的有效期 (EXP:) 已过,请勿使用 SKYRIZI。将产品退回药房。
- 如果预充式注射器掉落或损坏,请勿使用SKYRIZI 。请将产品退回药房。
- 如果纸盒穿孔破损,请勿使用SKYRIZI 。请将产品退回药房。
存储信息:
- 将 SKYRIZI 存放在36°F 至 46°F (2°C 至 8°C)的冰箱中。
- 不要摇晃 SKYRIZI。
- 将 SKYRIZI 放在原装纸盒中,避免光照,直至使用。
- SKYRIZI 不是采用天然橡胶乳胶制成的。
- 如果液体已冻结(即使已解冻),请勿使用。
请将 SKYRIZI 和所有药物放在儿童接触不到的地方。
如果您需要帮助或不知道如何继续,请致电您的医疗保健提供者或(866) SKYRIZI或(866) 759-7494。
|
洗净并擦干双手。 |
|
从 3 个可注射区域中选择:
|
|
握住预充式注射器,针头朝下,如图所示。
|
|
取下针盖。
|
|
一只手用拇指和食指握住预充式注射器的主体。另一只手 |
|
慢慢将柱塞杆推到底,直到所有液体都注入,注射器空了。保持注射器的角度不变,将针头从皮肤中拔出。
除非所有液体都已注入,否则针头保护装置不会自动启动。
|
|
使用第 2、3 和 4 个预充式注射器重复步骤 2 至 6,以获得全剂量。
|
|
使用后,请立即将用过的预充式注射器放入FDA 批准的锐器处理容器中。
如需更多信息,或如果您没有 FDA 批准的锐器容器,请参阅这些说明另一侧的“使用过的 SKYRIZI 预充式注射器处理”部分。 |
关于使用 SKYRIZI 注射器的问题
问: 如果我没有接受过医疗专业人员的面对面培训怎么办?
答:如果您需要帮助,请致电您的医疗保健提供者或(866) SKYRIZI或(866) 759-7494 。在注射前接受有关如何注射SKYRIZI 的培训。
问:注射后,我应该如何处理所有使用过的四支预充式注射器?
A. 将所有 4 个用过的预充式注射器扔进锐器处理容器中。不要扔进家庭垃圾中。有关更多信息,请参阅“用过的 SKYRIZI 预充式注射器处理”部分。
您可以访问 www.SKYRIZI.com 或致电 (866) 759-7494,注册获得用于 SKYRIZI 预充式注射器处置的锐器容器,无需支付额外费用
问:我如何知道注射何时完成?
A. 当预充式注射器为空、柱塞杆完全推入、注射器针头保护装置启动时,注射完成。
使用过的 SKYRIZI 预充式注射器处理
将所有四支用过的预充式注射器扔进锐器处理容器。不要扔进家庭垃圾中。
如果您没有经 FDA 批准的锐器处理容器,您可以使用以下家用容器:
- 由重型塑料制成,
- 可以用紧密贴合、防刺穿的盖子盖上,不会有尖锐物体掉出来,
- 使用过程中保持直立和稳定,
- 防漏,并且
- 已正确贴上标签,警告容器内有危险废物。
当您的锐器处理容器快要装满时,您需要遵循社区指南,以正确方式处理锐器处理容器。州或地方法律可能规定了如何丢弃用过的针头和注射器。
有关安全锐器处理的更多信息,以及您所在州的锐器处理的具体信息,请访问 FDA 网站:www.fda.gov/safesharpsdisposal。
请勿回收使用过的锐器处理容器。
制造商:AbbVie Inc.,美国伊利诺伊州北芝加哥 60064
美国许可证编号 1889
SKYRIZI ®是 AbbVie Biotechnology Ltd. 的商标。
© 2019-2024 AbbVie Inc.
本使用说明已获得美国食品药品管理局的批准。
修订日期:2024 年 3 月
使用说明
SKYRIZI ® (sky-RIZZ-ee) 体内注射器
Risankizumab-Rzaa
注射,仅供皮下使用
随身注射器和 180 mg/1.2 mL 预装药筒、
随身注射器和 360 mg/2.4 mL 预装药筒
在您开始使用 SKYRIZI 之前以及每次补充药物时,请阅读本使用说明。可能会有新信息。此信息不能代替与您的医疗保健提供者讨论您的医疗状况或治疗。
有关 SKYRIZI 产品信息,请参阅用药指南。 如需帮助,请致电您的医疗保健提供者、致电 (866) SKYRIZI 或 (866) 759-7494 或访问 SKYRIZI.com。
注射 SKYRIZI 前您需要了解的重要信息
- 在注射之前接受有关如何注射 SKYRIZI 的培训。
- 请勿摇晃 SKYRIZI 纸盒、体内注射器或预充药筒。
- 在准备注射之前,请勿从纸箱中取出体内注射器或预填充药筒。
- 将清洁的预充药筒装入随身注射器后,请勿等待超过 5 分钟才开始注射。等待会导致药物变干,之后随身注射器将无法工作。
- 在将装有预填充药筒的体内注射器放到皮肤上并准备注射之前,请勿
触摸开始按钮。◦您只能按一次开始按钮。
- 如果体内注射器或预填充药筒掉落或损坏,请勿使用。
- 请勿重复使用随身注射器或预装药筒。随身注射器和预装药筒仅供一次性(单剂量)使用。
- 请勿让体内注射器被水或任何其他液体弄湿。
- 此单剂量体内注射器仅适用于 SKYRIZI 预充药筒。
- 注射过程中应限制体力活动。可进行适度的体力活动,如散步、伸展和弯腰。
- 如果已超过有效期(EXP:),请勿使用 SKYRIZI。
- 如果液体变色、浑浊或含有薄片或大 颗粒,请勿使用预填充墨盒。液体应看起来清澈至黄色,可能含有微小的白色或透明颗粒。
- 体内注射器和预填充药筒不是采用天然橡胶乳胶制成的。
- 请将 SKYRIZI 和所有药物放在儿童接触不到的地方。
储存和使用准备
- 将 SKYRIZI 放在原装纸箱中,以防止使用前光线和物理损坏。
- 将 SKYRIZI 存放在 36°F 至 46°F (2°C 至 8°C) 的冰箱中。
- 准备使用时,将纸盒从冰箱中取出,并在室温下放置至少 45 分钟至 90 分钟, 以使 SKYRIZI 变暖。
- 如果将体内注射器放在室温下少于45 分钟,它就不会起作用。
- 请勿置于阳光直射下。
- 让 SKYRIZI 达到室温时,请勿从纸箱中取出体内注射器或预填充药筒。
- 请勿以任何其他方式加热 SKYRIZI。例如,请勿在微波炉或热水中加热。
- 如果液体已冻结(即使已解冻),请勿使用。
- 如果纸盒穿孔破损,请勿使用 SKYRIZI。请将产品退回药房。
- 如果白色纸盘密封丢失或损坏,请勿使用体内注射器和预填充药筒,并将纸箱退回药房。
了解您的 SKYRIZI 体内注射器和预充药筒




使用 SKYRIZI 前请阅读完整的使用说明。如果您需要帮助或不知道如何继续,请致电您的医疗保健提供者或 (866) SKYRIZI 或 (866) 759-7494 或访问 www.SKYRIZI.com。
步骤 1 做好准备 |
|
在使用 SKYRIZI 之前,您应该接受有关如何注射 SKYRIZI 的培训。 |
|
|
检查有效期
|
|
等待至少 45 分钟
|
|
打开纸箱,取出塑料托盘
|
|
收集所有用品并洗手
|
|
|
|
提起塑料盖
|
|
检查体内注射器
|
步骤 2 设置体内注射器 |
|
|
完全打开灰色门 避免接触针头盖或随身注射器背面的
|
|
检查预装墨盒
|
|
清洁预装墨盒较小的底部尖端
|
|
|
|
确保在将预充药筒插入随身注射器后 5 分钟内开始注射。等待会使药物变干,之后随身注射器将无法工作。 |
|
|
步骤 3 准备注射 |
|
注射完成前,请将手机等电子设备与体内注射器保持至少 12 英寸(30 厘米)的距离 |
|
|
选择注射部位
|
|
清洁注射区域
|
|
撕掉两个标签以露出粘合剂
|
|
|
|
准备放置体内注射器
|
|
将注射器放在皮肤上
|
步骤 4 注射药物 |
|
|
开始注射
|
|
注射过程中:
|
|
注射完成
|
|
|
步骤5 确认并处置 |
|
|
检查体内注射器
|
|
使用后立即将用过的随身注射器放入经 FDA 批准的锐器处理容器中
|

使用 SKYRIZI 前请阅读完整的使用说明。如果您需要帮助或不知道如何继续,请致电您的医疗保健提供者或 (866) SKYRIZI 或 (866) 759-7494 或访问 www.SKYRIZI.com。
常见问题
问:如果我无法打开体内注射器的门来插入预充药筒,该怎么办?
答: 要打开随身注射器门,请用力按压门左侧以释放门闩。如果您仍然无法打开门,请致电 (866) SKYRIZI 或 (866) 759-7494。
问:如果我在将体内注射器放到皮肤上之前按下灰色的开始按钮会怎么样?
答: 灰色启动按钮只能按一次。如果在佩戴前按下灰色启动按钮,则无法再使用。请致电 (866) SKYRIZI 或 (866) 759-7494。
问:如果我取下绿色拉环时,体内注射器没有发出蜂鸣声并且蓝色状态灯没有闪烁,该怎么办?
答:撕掉绿色小拉环即可取下透明塑料条,激活随身注射器。如果所有胶纸都已取下,但随身注射器仍无法启动,请致电 (866) SKYRIZI 或 (866) 759-7494。
问: 如果我将体内注射器放在皮肤上后按照说明按下开始按钮并且指示灯仍然是蓝色,会怎么样?
A. 再次用力按下灰色启动按钮。如果状态灯仍为蓝色或闪烁红色,请小心地将体内注射器从皮肤上剥离,将其取出。请勿重复使用体内注射器。请致电 (866) SKYRIZI 或 (866) 759-7494。
问:如果佩戴体内注射器时状态灯闪烁红灯并发出蜂鸣声怎么办?
答: 如果状态灯持续闪烁红色并发出哔哔声,请勿使用随身注射器。如果注射器附在身上,请小心取下。请致电 (866) SKYRIZI 或 (866) 759-7494。
问:如果注射过程中注射器脱落,我该怎么办?
答: 已装好的体内注射器不能再使用。请勿再次将其涂抹在身上。请致电 (866) SKYRIZI 或 (866) 759-7494。
问:我如何知道注射何时完成?
答: 当随身注射器发出蜂鸣声、白色柱塞完全填满药物窗口并且状态灯从闪烁的绿色变为常亮的绿色时,注射完成。
问:如果注射部位有几滴以上的液体,我该怎么办?
答. 致电 (866) SKYRIZI 或 (866) 759-7494 寻求帮助。
问: 注射后,我该如何处理用过的体内注射器?
答: 将使用过的随身注射器扔进 FDA 批准的锐器处理容器中,而不是扔进家庭垃圾中。您可以访问 www.SKYRIZI.com 或致电 (866) SKYRIZI 或 (866) 759-7494 免费获得用于 SKYRIZI 处理的锐器容器。
问:如果我没有接受过医疗专业人员的面对面培训怎么办?
答. 如果您需要帮助,请致电您的医疗保健提供者或 (866) SKYRIZI 或 (866) 759-7494。
在注射之前接受有关如何注射SKYRIZI 的培训。

处置 SKYRIZI
- 使用后立即将 SKYRIZI 放入经 FDA 批准的锐器处理容器中。请勿将 SKYRIZI 扔进(处理)家庭垃圾中。
- 如果您没有 FDA 批准的锐器处理容器,您可以使用符合以下要求的家用容器:
◦ 由重型塑料制成,
◦ 可以用紧密贴合、防刺穿的盖子关闭,而锐器不会掉出来,
◦ 使用时直立且稳定,
◦ 防泄漏,并且
◦ 正确贴有标签以警告容器内有危险废物。
当您的锐器处理容器快要装满时,您需要遵循社区指南,以正确方式处理锐器处理容器。州或地方法律可能规定了如何丢弃用过的针头和注射器。
有关您所在州的安全锐器处理的更多信息,请访问 FDA 网站:www.fda.gov/safesharpsdisposal。
请勿回收使用过的锐器处理容器。
附加信息
● BF 型应用部分。
● 体内注射器采用环氧乙烷消毒。
体内注射器采用环氧乙烷消毒。
● 高度范围为 -1,312 英尺至 10,499 英尺(-400 米至 3,200 米)。
体内注射器的电磁兼容性 (EMC)
体内注射器适合家庭使用或专业医疗环境中使用,符合 ISO 11608-1:2014 和 IEC 60601-1-2:2014 标准。
应注意在以下特定限制和环境下使用体内注射器,以避免对性能产生不利影响(错过或不完整的 SKYRIZI 剂量)。
- 注射完成前,请将手机等电子设备与随身注射器保持至少 12 英寸(30 厘米)的距离。在 12 英寸(30 厘米)范围内操作随身注射器时,电子干扰的潜在影响尚不清楚。
- 请勿将体内注射器暴露于磁共振 (MR) 环境 (例如 MRI)。
- 如果在其他电气设备附近使用,请观察随身注射器和其他设备,以确保其正常运行。
排放
| 排放测试名称 | 测试级别 |
| 辐射射频电磁场 | 符合 CISPR 11,B 类标准 |
电磁抗扰度
| 测试名称 | 测试级别 |
| 静电放电 (ESD) | ± 8 kV 接触放电 ± 2 kV, ± 4 kV, ± 8 kV, ± 15 kV 空气放电 |
| 射频电磁场 | 10 伏/米 80 兆赫 – 2.7 千兆赫 |
| 工频50Hz磁场 | 30安/米 |
外壳端口对射频无线通信设备的抗干扰能力符合 IEC 60601-1-2:2014 标准。
符号词汇表
象征 |
符号说明 |
|
保持干燥 |
|
使用环氧乙烷灭菌 |
|
请勿重复使用 |
|
如果包装损坏,请勿使用,并参阅使用说明 |
|
生产日期 |
|
批次代码 |
|
目录编号 |
|
序列号 |
|
请参阅说明书/手册 |
|
BF型应用部分 |
|
不安全先生 |
制造商:
AbbVie Inc.,美国伊利诺伊州北芝加哥 60064
美国许可证编号 1889
SKYRIZI® 是 AbbVie Biotechnology Ltd. 的注册商标。
©2024 AbbVie Inc.
本使用说明已获得美国食品药品监督管理局的批准。
修订日期:6/2024
20086115
NDC 0074-2100-01
一支 1 毫升单剂量预充注射笔
Skyriz i® PEN 150 毫克/毫升
risankizumab-rzaa 注射液
仅供皮下使用
如果纸盒穿孔破损,请退回药房。
药剂师请注意:
每位患者都必须接受
随附的用药指南。
整个纸箱作为一个整体进行分发。
药品标签区域
www.SKYRIZI.com
仅限 Rx
艾比

NDC 0074-1050-01
一支 1 毫升单剂量预充式注射器
Skyriz i ® 150 毫克/毫升
利桑基祖玛布扎
注射
仅供皮下使用
如果纸盒穿孔破损,请退回药房。
整个纸箱作为一个整体进行分发。
药品标签区域
www.SKYRIZI.com
仅限 Rx
艾比

NDC 0074-1070-01
1 x 2.4毫升预填充墨盒
思瑞兹
risankizumab-rzaa 注射液
(3 60毫克 / 2.4毫升)
150毫克/毫升
仅供皮下使用
单剂量
SKYRIZI.com
仅限 Rx
艾比

NDC 0074-5015-01
思瑞兹
risankizumab-rzaa 注射液
600毫克/ 10毫升
(60 毫克/毫升)
仅供静脉内使用
使用前必须稀释
一瓶 10 毫升单剂量药瓶 -
丢弃未使用的部分
注意:向每位患者分发随附的用药指南。
仅限 Rx
艾比

NDC 0074-1069-01
舒利齐
里桑基祖玛布扎
注射
360 毫克/2.4 毫升
(150毫克/毫升)
仅供皮下使用
单剂量
仅限 Rx

NDC 0074-1069-02
非卖品
舒利齐
里桑基祖玛布扎
注射
360 毫克/2.4 毫升
(150毫克/毫升)
仅供皮下使用
单剂量
仅限 Rx

NDC 0074-1065-01
1 x 1.2 毫升预填充墨盒
1 个体内注射器
舒利齐
risankizumab-rzaa 注射液
(180 毫克/1.2 毫升)
150毫克/毫升
仅供皮下使用
单剂量
SKYRIZI.com
仅限 Rx
艾比

NDC 0074-1066-01
舒利齐
里桑基祖玛布扎
注射
180 毫克/1.2 毫升
(150毫克/毫升)
仅供皮下使用
单剂量
仅限 Rx

NDC 0074-1066-02
非卖品
舒利齐
里桑基祖玛布扎
注射
180 毫克/1.2 毫升
(150毫克/毫升)
仅供皮下使用
单剂量
仅限 Rx

NDC 0074-7034-02
2 x 1 毫升预充式注射器
思瑞兹
risankizumab-rzaa 注射液
每注射器 90 毫克/毫升
2 x 90 毫克/毫升。单剂量预充式
总剂量为 180 mg/2 mL 的注射器
仅供皮下使用
仅供医疗服务提供者管理
www.SKYRIZI.com
仅限 Rx
艾比

NDC 0074-7032-90
一支 1 毫升单剂量预充式注射器
思瑞兹
risankizumab-rzaa 注射液
90毫克/毫升
仅供皮下使用
仅供医疗服务提供者管理
www.SKYRIZI.com
仅限 Rx
艾比

NDC 0074-7036-04
4 x 1 毫升预充式注射器
思瑞兹
risankizumab-rzaa 注射液
每注射器 90 毫克/毫升
4 x 90 毫克/毫升单剂量预充式
总剂量为 360 mg/4 mL 的注射器
仅供皮下使用
仅供医疗服务提供者管理
药剂师请注意:
每位患者均须收到随附的用药指南。
整个纸箱将作为一个单位进行分配。
如果纸箱密封破损或丢失,请退回药房。
www.SKYRIZI.com
仅限 Rx
艾比

NDC 0074-7032-01
Skyrizi® 90毫克/毫升
利桑基祖玛布扎
注射
仅供皮下使用
仅供医疗服务提供者管理
对于 350 毫克剂量,
需要四支 90 毫克注射器,
注射全部 4 个注射器以获得完整剂量
www.SKYRIZI.com
仅限 Rx
艾比

NDC 0074-7040-02
2 x 90 毫克/毫升单剂量预充式注射器
思瑞兹
每注射器 90 毫克/毫升
2 x 90 毫克/毫升单剂量预充液
总剂量为 180 mg/2 mL 的注射器
利桑基祖玛布扎
注射
仅供皮下使用
如果纸盒穿孔破损,请退回药房。
药剂师请注意:
每位患者都必须接受
随附的用药指南。
整个纸箱作为一个整体进行分发。
对于 180 毫克剂量,
需要两支 90 毫克注射器。
注射 2 支注射器即可获得完整剂量。
www.SKYRIZI.com
仅限 Rx
艾比

| SKYRIZI risankizumab-rzaa 试剂盒 |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| SKYRIZI risankizumab-rzaa 注射剂 |
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
| SKYRIZI risankizumab-rzaa 注射剂 |
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
| SKYRIZI risankizumab-rzaa 试剂盒 |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| SKYRIZI risankizumab-rzaa 注射剂 |
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||
| SKYRIZI risankizumab-rzaa 试剂盒 |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| SKYRIZI risankizumab-rzaa 试剂盒 |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| SKYRIZI risankizumab-rzaa 试剂盒 |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| SKYRIZI risankizumab-rzaa 试剂盒 |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| SKYRIZI risankizumab-rzaa 试剂盒 |
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
|
||||||||||||||||||||
| 标签机 - AbbVie Inc. (078458370) |
- 名 称:
- Skyrizi
- 全部名称:
- Skyrizi、利生奇珠单抗、瑞莎珠单抗
- 上市状态:
- 美国2019年 申请上市获得受理
- 生产药企:
- 艾伯维(AbbVie)
- 规格:
- 150 mg/mL 预填充注射器和笔、用于静脉输注的 600 mg/10 mL 小瓶和180 毫克/1.2 毫升或带贴体注射器的 360 mg/2.4 mL 单剂量预填充盒。
- Skyrizi与Ilumya有何区别? 2024-11-07
- Skyrizi与Humira治疗斑块状银屑病的比较? 2024-11-07
- 服用Skyrizi期间可以饮酒吗? 2024-11-07
- 斯Kyrize(Skyrizi)是否获批用于治疗银屑病关节炎? 2024-11-07
- 谁生产Skyrizi?它在哪里生产? 2024-11-07
- 如何给予斯奇瑞兹(Skyrizi)注射? 2024-11-07
- Skyrizi的作用机制(MOA)? 2024-11-07
- 瑞莎珠单抗会导致脱发吗? 2024-11-07
- Skyrizi的用药方案是什么? 2024-11-07
- 瑞莎珠单抗(Skyrizi)会导致癌症吗? 2024-11-07
- Skyrizi起效需要多长时间? 2024-11-07
- 什么是单克隆抗体? 2024-11-07
- Risankizumab药物全解与使用攻略 2024-09-13
- Risankizumab治银屑病和银屑病关节炎:用法和注意事项 2024-09-13
- Skyrizi(利善扎尤单抗):超详细的药物点评 2024-09-13
- Skyrizi针剂全攻略:效果、副作用和用法大揭秘 2024-09-13
- Skyrizi(Risankizumab)现在可以用来治牛皮癣、关节炎和克罗恩病啦! 2024-09-13







































































